国际输血医学最新动态2025年第11期
红细胞血型抗体和不相容输血的抗原调节与清除机制
中国输血协会临床输血管理学专业委员会组稿
深圳市第二人民医院输血科组织编译
引 言
本期《输血医学新进展》聚焦红细胞血型抗体的产生和不相容输血的抗原调节与清除机制,通过分享3篇相关文章,展示了近年该领域的一些研究成果,内容涵盖小鼠对输注同种异体红细胞的先天性和适应性免疫反应依赖于MyD88,I型干扰素依赖和非依赖狼疮小鼠模型中不同的红细胞同种抗体反应,以及CD47调控不相容输血后抗原调节及红细胞清除。这些研究成果具有重要意义:1)储存的红细胞(RBC)通过依赖MyD88的信号通路激活常规树突状细胞(cDCs),提示TLR介导的信号决定了RBC输注是否能够引发促同种异体免疫的炎症反应。揭示了RBC同种异体免疫中关键的免疫信号通路,为进一步识别触发免疫应答的RBC相关配体提供了基础,也为开发针对性的RBC同种异体免疫防控策略奠定了理论依据。2)I型干扰素是狼疮患者红细胞同种免疫的关键因素,未来可以通过检测I型干扰素相关标志物,为SLE患者制定 “量体裁衣”的输血方案,有望大幅降低输血相关并发症的发生,提升患者诊疗的安全性,让输血治疗既“有效”又“安全”。3)CD47在调控红细胞清除和抗体介导的调节过程中起着重要作用,提示CD47可能是调节红细胞在不相容输血后抗体介导清除结果的关键特征,在无法获得完全相容红细胞的情况下,利用这一结果可能有助于增强靶抗原的变化,从而优先调节抗原。这些新的研究成果为红细胞血型同种免疫的预防与安全输血提供了新的理论依据。
小鼠对输注同种异体红细胞的先天性和适应性免疫反应
依赖于MyD88
编译:叶至顺 廖奇峰 审校:伍昌林
1 研究背景
长期红细胞输注是治疗多种血液系统疾病及骨髓衰竭综合征(如镰状细胞贫血、重型地中海贫血和骨髓增生异常综合征)的重要手段。然而,红细胞输注的一个主要并发症是产生非ABO血型系统的同种抗体。与针对A和B血型抗原的天然IgM抗体不同,非ABO同种抗体是在输血或妊娠后针对供体红细胞上的多态性次要抗原产生的。临床上,大约3-10%的输血患者会发生红细胞同种异体免疫反应,而在需长期反复输血的患者中,这一比例可高达50%。红细胞同种异体免疫可能引起溶血性输血反应,这种反应具有潜在的致命性,并会因寻找相容血液而延迟输血时间。除尽量避免输血外,目前尚缺乏有效的干预措施以防止RBC同种异体免疫。尽管其临床意义重大,但RBC输注后同种异体抗体形成的机制仍未完全阐明。
2 主要研究结果
2.1储存红细胞可激活树突状细胞并诱导同种异体抗体反应
采用一种模拟人类输血过程的转基因小鼠模型(HOD),包含鸡卵白溶菌酶(HEL,B细胞表位)、卵清蛋白(OVA,T细胞表位)以及人红细胞小抗原 Duffy^b(图1A)。该模型能够在输血过程中精确解析引发有害同种免疫反应所需的受体及信号通路。将 HOD 红细胞按与临床储血相似的条件在4℃ 储存后,可用于研究针对模型红细胞抗原的先天和适应性免疫反应。经过无菌处理并在 4℃ 储存12天的HOD 红细胞,在输注至野生型(WT)C57BL/6小鼠后,可诱导强烈的抗 HOD 同种异体抗体反应;新鲜(未储存)HOD 血液输注后仅产生极少量抗体,其水平与未输血的对照小鼠相似(图1B)。结果显示,储存的(而非新鲜的)HOD RBC 输注至C57BL/6 受体后,可在输后6小时诱导脾脏 cDC2上CD86 表达的显著升高(图1C)。与HOD红细胞类似,将储存的C57BL/6小鼠红细胞(即同基因红细胞)输注至C57BL/6小鼠,也发现其可诱导cDC2s表达CD86,而新鲜红细胞则无此作用(图1D)。这表明cDC2s的先天免疫激活并不依赖于红细胞上是否存在同种抗原。在已产生HOD抗体的小鼠中输注新鲜红细胞,发现其仍无法激活cDC2s,说明即使在已有免疫反应的背景下,HOD抗原本身也不足以激活cDC2s。最后,发现储存红细胞本身(而非其储存上清)含有相关的先天免疫刺激物,因为将储存红细胞用无菌PBS稀释后输注可激活cDC2s,而单独输注储存过程中产生的上清液则无此作用(图1E)。无论是否存在同种抗原,输注储存红细胞均可诱导cDC2s从桥通道迁移至白髓TCZ;而在未处理或输注新鲜红细胞的小鼠中未观察到该现象(图1F–G)。表明储存红细胞即使在没有外源抗原的情况下,也能诱导DC激活,从而启动适应性免疫反应。

图1. 储存红细胞可激活树突状细胞并诱导同种异体抗体反应。
2.2储存红细胞诱导的细胞因子反应、树突状细胞活化与同种抗体形成依赖于 MyD88和TRIF 信号通路
此前结果已排除NLR受体家族在该过程中发挥作用的可能性,因此进一步考虑TLR 受体是否参与储存红细胞的免疫识别。由于所有TLR信号传导均依赖适配蛋白TRIF和/或MyD88,首先在Trif-/- Myd88-/-双敲小鼠中进行验证。与WT小鼠相比,Trif-/-Myd88-/-小鼠在输注储存RBC后,其血清炎性细胞因子 IL-6、CXCL1(又称KC)和 CCL2(又称MCP-1)显著下降(图 2A)。输血6小时后,Trif-/-Myd88-/-小鼠脾脏 cDC2 的 CD86 表达未见上调(图 2B)。此外,该双敲小鼠在输血21天后的抗HOD 抗体滴度与未输血小鼠相当(图 2C),提示其适应性免疫应答受损。为区分 MyD88与TRIF的独立作用,进一步分别在Myd88-/-与Trif-/-小鼠中进行实验,不同的 PRRs 可通过不同的适配蛋白介导独特的下游信号。

图2. 储存红细胞诱导的细胞因子反应、树突状细胞活化与同种抗体形成依赖于MyD88 和 TRIF信号通路。
2.3储存红细胞诱导的同种免疫依赖MyD88而非TRIF
实验结果显示,与WT小鼠不同,Myd88-/-小鼠在输注储存RBC后2小时内几乎不产生 CCL2(图3A);而Trif-/-小鼠的 CCL2 水平与WT无显著性差异(图 3B)。这表明MyD88而非TRIF对储存RBC诱导的早期固有免疫反应至关重要。进一步检测发现,Myd88-/-小鼠在储存HOD RBC 输注后未能形成抗 HOD 同种异体抗体(图3C);相反,Trif-/-小鼠的抗体水平与WT相当(图3D)。因此,依赖TRIF信号(如TLR3)的受体并非储存RBC诱导同种免疫所必需。随后我们探讨哪类细胞依赖MyD88信号介导储存 RBC的活化反应。我们在输血后6小时检测多种脾脏免疫细胞的 CD86表达,以评估其对储存RBC的应答。结果显示,储存RBC并不直接激活滤泡性 B 细胞或边缘区B细胞。在先天免疫细胞中,仅常规 DC亚群(cDC1与cDC2)表现出强烈的CD86 上调(图4A),而单核细胞及浆细胞样DC(pDC)均未显著激活(图4A)。由些表明MyD88是一种具有多重功能的信号适配分子,在先天及适应性免疫通路中均发挥关键作用。

图 3. 储存红细胞诱导的同种免疫依赖 MyD88 而非TRIF。
2.4储存红细胞诱导的树突状细胞(DC)活化与迁移依赖 MyD88 信号通路
在Myd88-/-小鼠中,cDC 亚群的CD86上调完全被阻断(图 4A),表明其活化依赖功能性 MyD88 信号。尽管巨噬细胞在WT 与敲除鼠间存在统计学差异,但总体活化水平远低于 cDC,因此生物学意义有限;此外,实验采用的脾脏机械消化方法偏向提取 cDC,对大体积巨噬细胞回收率较低,亦可能影响结果解释。我们此前已证实,cDC2是储存 RBC 诱导同种抗体产生的关键DC亚群,其作用部分源于迁移至白髓CD4?T细胞区的能力。在本研究中,我们观察到,Myd88-/-小鼠在储存 RBC 输注后6小时内,cDC2 向白髓迁移显著受阻,与对照组相比明显减少(图4B)。这进一步支持了储存RBC诱导的cDC2活化依赖于MyD88信号通路的结论。

图4. 储存红细胞诱导的树突状细胞(DC)活化与迁移依赖 MyD88 信号通路。
3 主要结论
1)本研究验证了储存红细胞(RBC)而非新鲜红细胞能够通过依赖 MyD88 而非TRIF的信号通路激活常规树突状细胞(cDCs)。这一发现提示TLR介导的信号决定了RBC输注是否能够引发同种异体免疫的炎症反应。
2)储存的C57BL/6小鼠红细胞本身具备内在免疫原性,即便不携带外源表位,也能诱导DC成熟。因此,在常规储存条件下,RBC可通过MyD88依赖性机制获得免疫原性,并激活免疫反应。
3)这些发现揭示了RBC同种异体免疫中关键的免疫信号通路,为进一步识别触发免疫应答的RBC相关配体提供了基础,也为未来开发针对性的RBC同种异体免疫防控策略奠定了理论依据。
4 文献来源
Arielle Soldatenko , Laura R Hoyt, Lan Xu,et al. Innate and Adaptive Immunity to Transfused Allogeneic RBCs in Mice Requires MyD88. J Immunol.2022; 208(4):991-997. doi: 10.4049/jimmunol.2100784.
I型干扰素依赖和非依赖狼疮小鼠模型中不同的红细胞同种抗体反应
编译:胡晓榕 蔡仲仁 审校:伍昌林
1 研究背景
红细胞输血是临床救治贫血、失血的重要手段,但输血过程中,受血者会接触到供体红细胞上的ABO及360余种非ABO“次要抗原”(如Kell、Duffy抗原)。由于临床常规仅匹配ABO和Rh(D)血型,非ABO抗原极易引发受血者产生 “红细胞同种抗体”,进而可能导致严重的溶血性输血反应(美国 FDA 数据显示,非ABO抗体相关溶血是输血致死的主要原因之一),还会限制后续匹配血源的获取,对需要反复输血的患者尤其不利。而SLE患者作为“高风险群体”,面临的矛盾更为突出:约50%SLE患者合并贫血,对输血需求更高;超过半数成人SLE患者及几乎所有儿童SLE患者,体内存在I型干扰素相关基因高表达,且该特征与自身抗体产生、疾病严重程度密切相关;此前研究已证实,I型干扰素可促进病毒感染或炎症状态下的红细胞同种免疫,但它在狼疮患者中的作用,始终未与“狼疮样病理改变”明确区分。为解答这一关键问题,研究团队设计了核心实验:同时使用两种机制截然不同的狼疮小鼠模型,对比分析I型干扰素与狼疮表型对红细胞同种免疫的影响。
2 主要研究结果
2.1 MRL-lpr和降植烷诱导的狼疮小鼠的自身免疫性病理学
使用降植烷诱导的狼疮小鼠(IFNα/β依赖型)和MRL-lpr小鼠(IFNα/β非依赖型)来确定狼疮样病理对红细胞同种免疫反应的影响。对野生型(WT)小鼠、用降植烷(PrWT)处理的WT小鼠和MRL-lpr小鼠的脾脏白细胞进行了定量。与未经治疗的野生型小鼠相比,MRL-lpr小鼠的脾细胞、脾B和T细胞水平升高(图1A-C)。与WT小鼠相比,PrWT小鼠和MRL-lpr小鼠的狼疮相关抗sDNA自身抗体数量增加(图1D)。肾脏组织学检查显示,老年MRL-lpr小鼠(6-9 月龄)以及在分析前 6-9个月接受过降植烷处理的 PrWT 小鼠,均出现轻度肾小球系膜区扩张与系膜细胞增生。与WT小鼠相比,两组狼疮样小鼠均表现出显著升高的肾脏病理学评分。然而,MRL-lpr和PrWT小鼠之间没有显著差异(图1E,F)。这些数据表明,在IFNα/β依赖型和非依赖型狼疮模型中都存在狼疮样病变。
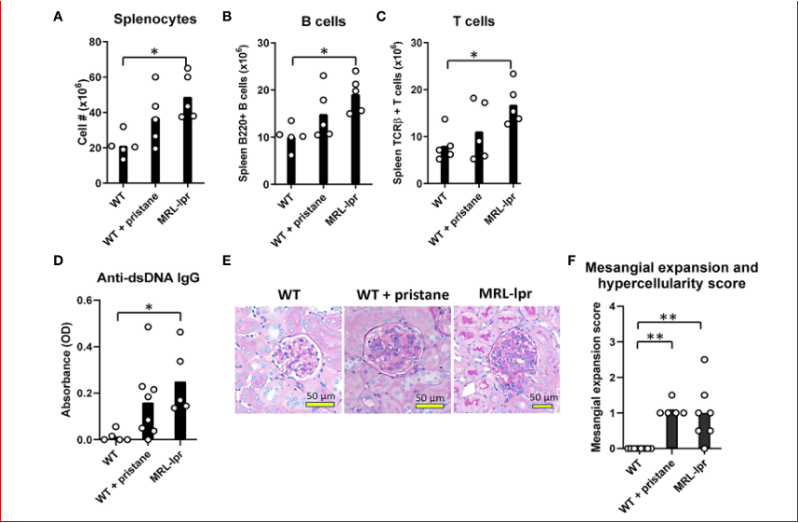
图1. 降植烷诱导和MRL-lpr小鼠模型中的炎症和狼疮样表型
2.2 MRL-lpr和PrWT狼疮小鼠的抗KEL同种免疫
给WT小鼠、输血前14天注射降植烷的PrWT小鼠和MRL-lpr小鼠输注表达KEL1抗原的去白细胞红细胞(K1小鼠)。通过流式细胞仪交叉配血测定抗KEL IgM水平(输血后5天)和峰值抗KEL IgG水平(输血后21天)。抗-KEL IgM水平没有显著差异。然而,与野生型和MRL-lpr小鼠相比,PrWT小鼠产生了显著更高水平的抗-KEL IgG(图2A,B)。与WT小鼠相比,PrWT小鼠每种抗-KEL IgG亚型的水平显著更高。与野生型小鼠相比,MRL-lpr小鼠产生了较高量的IgG2c,而其他亚型的水平在MRL-lpr和未治疗的野生型小鼠之间是相当的(图2C)。为探究抗-KEL抗体的影响,作者检测了 K1型红细胞(RBCs)从外周血循环中被清除的程度。初次输注 K1 RBCs 35 天后,向三组小鼠再次输注荧光标记的 K1 RBCs(DiI 标记)与同源 WT RBCs(DiO 标记),通过流式细胞术检测4天内循环中两种红细胞的比例(即 “输血后回收率”),结果显示:PrWT 小鼠循环中 DiI+ K1 RBCs 比例显著降低,约 50% 的 K1 RBCs 被清除,表现出对 K1 RBCs 的特异性清除能力;而WT小鼠、MRL-lpr小鼠:循环中 DiI+ K1 RBCs与 DiO+WT RBCs 比例无显著变化,未表现出对 K1 RBCs 的特异性清除;阴性对照(未产生抗 KEL 抗体的 naive K1 转基因小鼠):同样无 K1 RBCs 特异性清除现象(图2D)。
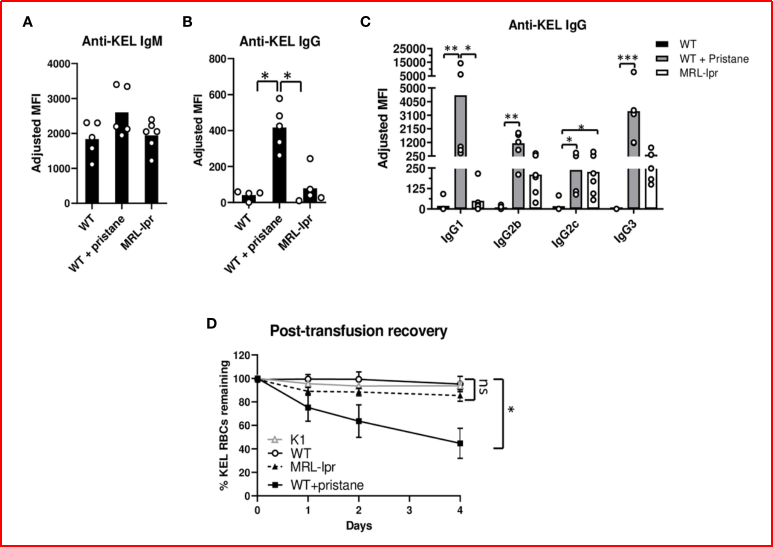
图2. 降植烷诱导抗-KEL抗体
2.3 MRL-lpr狼疮鼠产生针对可溶性抗原的抗体
由于MRL-lpr小鼠在红细胞输注后产生最低水平的抗-KEL IgG,作者检测了MRL-lpr小鼠对可溶性抗原免疫应答的程度。用乳化在明矾中的NP-KLH初次免疫后,分别在免疫后5天和7-28天测量了抗NP IgM和抗NP IgG水平。MRL-lpr和WT小鼠产生的抗NP IgM水平相当。MRL-lpr 小鼠与野生型(WT)小鼠均能产生抗 NP IgG,只是产生动力学略有不同。免疫后 7 天,野生型小鼠的抗 NP IgG 水平高于 MRL-lpr小鼠;但在免疫后 14 天、21 天和 28 天,两组小鼠的抗 NP IgG 水平无显著差异(图3A、B)。在初次免疫后 35 天,用 NP-KLH加强免疫后,野生型小鼠与 MRL-lpr 小鼠的抗 NP IgG 水平仍无显著差异(图 3C)。尽管与野生型小鼠相比,MRL-lpr 小鼠产生抗 NP IgG 的过程存在延迟,但这些结果表明,MRL-lpr小鼠能够产生针对可溶性抗原的IgG 抗体。
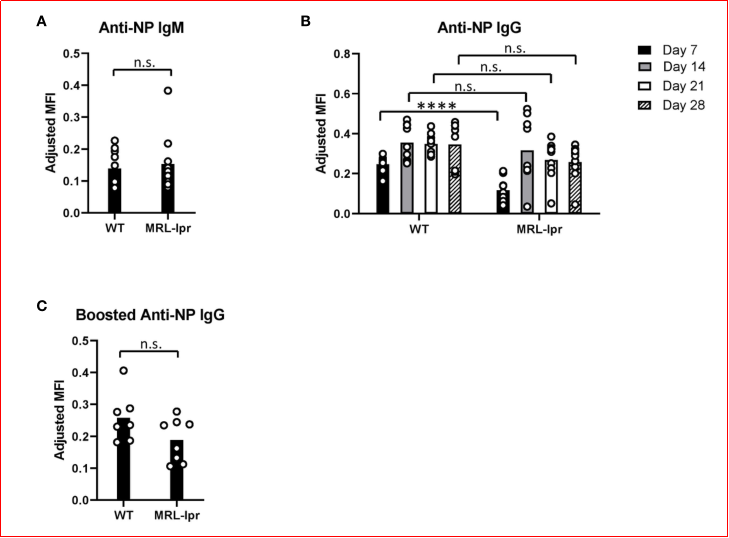
图3. 用可溶性抗原免疫后的抗NP抗体
2.4 狼疮模型围输血期的炎症反应
为了评估同种免疫反应,在输血时测量各种血清细胞因子的水平。与未处理的WT对照组相比,MRL-lpr小鼠表现出更高数量的CCL5和CXCL1细胞因子,而PrWT小鼠与WT小鼠相比产生更高浓度的CXCL1和CCL2(图4A)。与未处理的WT小鼠相比,PrWT小鼠表现出IFNβ和IFNα水平升高,而MRL-lpr小鼠中的IFNα/β水平与未处理的WT小鼠中的水平没有显著差异(图4B)。由于小鼠血清中干扰素 α(IFNα)和干扰素 β(IFNβ)具有短暂性,文中在输血时还检测了干扰素 α/β 诱导基因(ISGs)。与野生型(WT)小鼠和MRL-lpr小鼠相比,PrWT小鼠血清中干扰素诱导基因产物 IP-10的浓度较高(图 4C)。通过实时定量 PCR 检测脾脏单核细胞中 Mx1、ISG15、IRF7(均为 I 型干扰素通路关键基因)的转录水平,结果显示:PrWT 小鼠:Mx1、ISG15 转录水平显著高于 WT 小鼠和 MRL-lpr 小鼠,IRF7 转录水平显著高于 WT 小鼠;MRL-lpr 小鼠:上述 3 种基因转录水平与 WT 小鼠无显著差异,未出现 I 型干扰素通路激活(图 4D)。图4A-D表明证实I型干扰素是两种模型免疫反应差异的关键变量。向 WT小鼠和MRL-lpr小鼠输注 K1 RBCs 时,同步加入或不加入重组 IFNα(rIFNα),检测 7 天后的抗 KEL IgG 水平,结果显示加入 rIFNα 的WT小鼠和 MRL-lpr小鼠的抗-KELIgG水平均显著高于未加入 rIFNα的同模型小鼠。原本抗-KEL IgG 水平极低的 MRL-lpr 小鼠,在补充 rIFNα 后,同种抗体产生能力明显增强(图 4E),证实 I 型干扰素与红细胞同种免疫的因果关系。
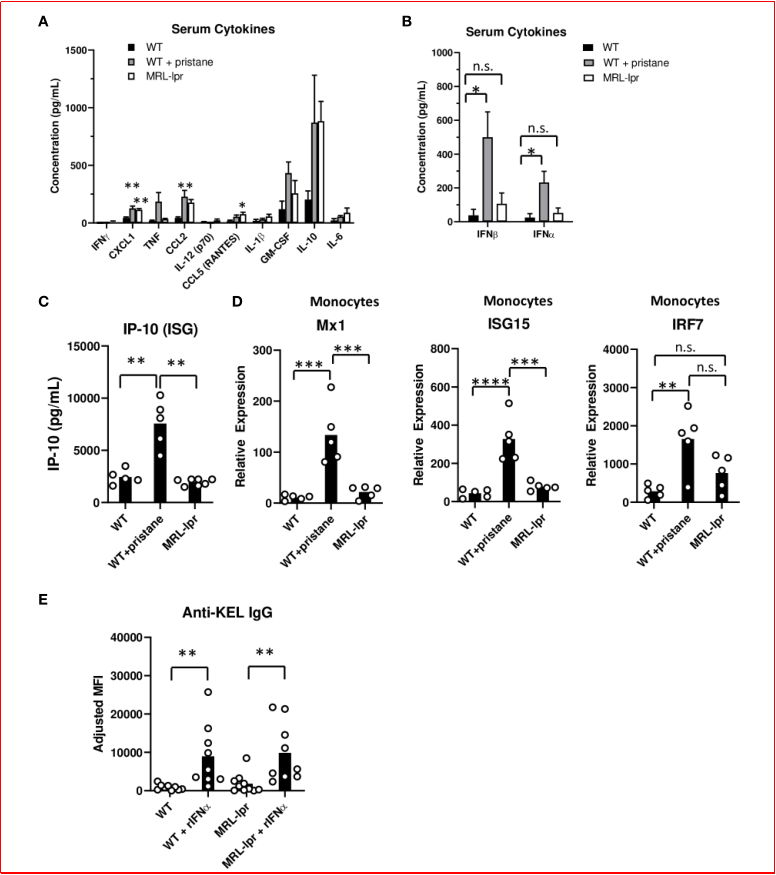
图4. 降植烷诱导的和MRL-lpr小鼠模型中的炎症和ISG表达
3 主要结论
I型干扰素是狼疮患者红细胞同种免疫的关键因素。未来可以通过检测I型干扰素相关标志物,为SLE患者制定“量体裁衣”的输血方案,有望大幅降低输血相关并发症的发生,提升患者诊疗的安全性,让输血治疗既“有效”又“安全”。
4 文献来源
Kausik Paul , Rosario Hernández-Armengol , June Young Lee,et al. Distinct RBC alloantibody responses in type 1 interferon-dependent and -independent lupus mouse models. Front Immunol. 2024:14:1304086. doi: 10.3389/fimmu.2023.1304086.
编译:刘凌云 黄海燕 审校:伍昌林
1 研究背景
输血是临床中最常见的治疗手段之一,但个体之间红细胞表面抗原的差异可能引发异体抗体的产生。由于异体抗体在输血时可能未被检测到,当患者再次接触到之前已经产生免疫反应的红细胞异体抗原时,可能引发复发性异体免疫反应,从而导致输注红细胞的加速清除,这种反应构成了迟发性溶血性输血反应。但有研究表明,红细胞在不相容输血后并不总是会被清除。这种现象发生的原因可能有多种,但抗体诱导靶抗原改变的能力已成为不相容红细胞输血的独特结果,即使没有检测到任何红细胞清除,也可能发生这种改变。这种现象被称为抗体诱导的抗原调节,它可以减少红细胞表面可检测到的抗体水平,通常使红细胞对进一步的抗体介导的清除变得不敏感,但调控抗体介导的抗原丧失的因素仍然未知。红细胞上表达的CD47是一种抗吞噬标记,CD47可通过与SIRPα的相互作用来防止细胞被清除,输注红细胞上的CD47水平可能在不兼容输血的结果中发挥重要作用。抗体诱导的红细胞清除与CD47介导的信号之间的相互作用可能在一定程度上决定了抗体结合输注红细胞后,是发生抗原调节还是红细胞清除。鉴于不相容红细胞输血对患者结果的影响,本文探讨了CD47作为抗体介导的抗原调节和红细胞清除的调节因子的作用。
2 主要研究结果
2.1 CD47基因敲除和杂合HOD红细胞(RBCs)具有降低的CD47水平,同时HOD抗原水平相当。
创建具有不同CD47水平(野生型、杂合子或敲除型)的供体小鼠(图1A、B)。首先使用一组单克隆抗体,针对HEL抗原上的不同表位,评估每个供体组(HOD CD47 WT、HOD CD47 HET和HOD CD47 KO)的HOD抗原水平。通过这种方法,未观察到供体组之间HEL水平的显著差异,提示在CD47 WT、CD47 HET和CD47 KO HOD红细胞供体中,HEL抗原水平保持相似(图1B-E)。网织红细胞数量的差异不足以引起来自三个供体的红细胞中整体HEL水平的差异(图1B-E),观察到CD47 WT、CD47 HET和CD47 KO HOD红细胞上HEL抗原的水平相似(图1E)。使用抗-HEL抗体组合进一步检测HOD抗原也得出了相似的结果,CD47的表达水平与基因剂量相关(图1F、G)。来自CD47杂合小鼠(HOD CD47 HET)的红细胞表达的CD47水平大约是来自纯合子供体(HOD CD47 WT)红细胞的CD47水平的一半。相反,来自CD47 KO小鼠的红细胞未能检测到CD47(图1F、G)。这些发现表明,将HOD红细胞模型与CD47 KO小鼠杂交可以生成具有不同CD47水平(WT、HET或KO)但保持相似HOD抗原水平的供体红细胞。
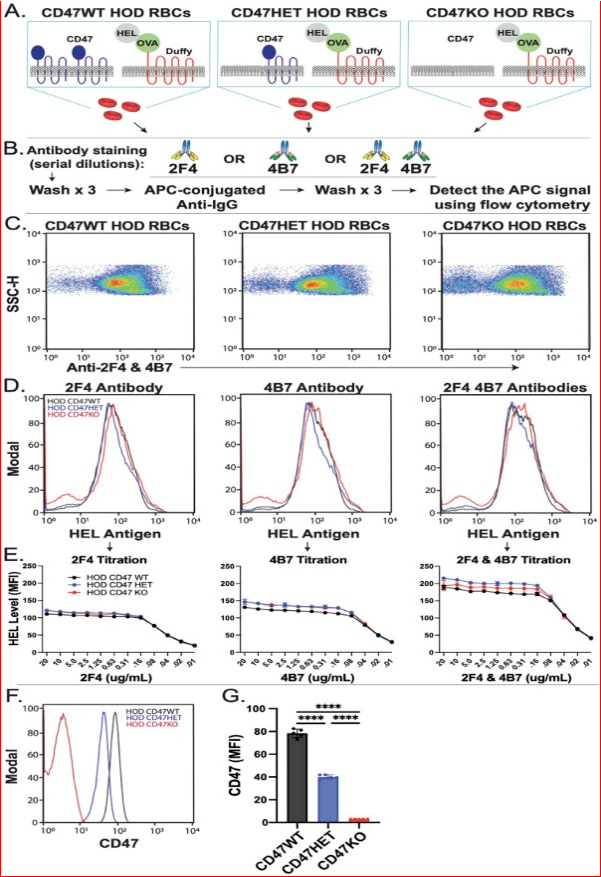
图1. CD47基因敲除和杂合HOD红细胞(RBCs)具有降低的CD47水平,同时HOD抗原水平相当。
2.2抗-HEL抗体增强HOD CD47杂合和敲除红细胞的清除,但对HOD CD47 WT红细胞的去除没有影响。
HOD CD47 WT、CD47HET或CD47KO红细胞使用荧光染料DiI标记,HOD抗原阴性红细胞使用另一种荧光染料DiO标记(图2A、B)。与先前的研究结果一致,将HOD CD47 WT红细胞输注到已注射抗-HEL抗体的受体中未能影响红细胞的清除,无论使用何种抗-HEL抗体,甚至在受体接受了组合型抗-HEL抗体时也未见影响(图2C-E)。当将HOD CD47 HET红细胞输注到未免疫的受体中时,尽管表达的CD47水平仅为一半,但未检测到红细胞存活的显著差异(图2C-E)。当将相同的HOD CD47 HET红细胞输注到仅被一种抗-HEL单克隆抗体动员的受体中时,结果也相似(图2C-E)。当将HOD CD47 HET红细胞输注到已接受组合型抗-HEL抗体免疫的受体中时,可以检测到加速的红细胞清除(图2C-E)。采用与前述相同的方法标记HOD CD47 KO红细胞,并将其输注到未免疫或抗-HEL免疫的受体中。与HOD CD47 WT或HOD CD47 HET红细胞不同,后者在缺乏抗-HEL抗体的情况下输血后未表现出明显的存活差异,HOD CD47 KO红细胞在输注到未免疫受体后显示出存活率下降(图2C-E)。与HOD CD47 HET红细胞输注的结果相比,HOD CD47 KO红细胞在仅接受单一单克隆抗-HEL抗体免疫的受体中被加速清除(图2C-E)。在接受了两种抗-HEL抗体免疫的受体中,清除速率更加明显,这一差异在与未接种抗-HEL抗体的清除速率标准化后更加显著(图2C-E)。这些结果表明,CD47不仅可能调节红细胞的存活,而且可能影响在不兼容输血后抗体结合对红细胞清除的影响。
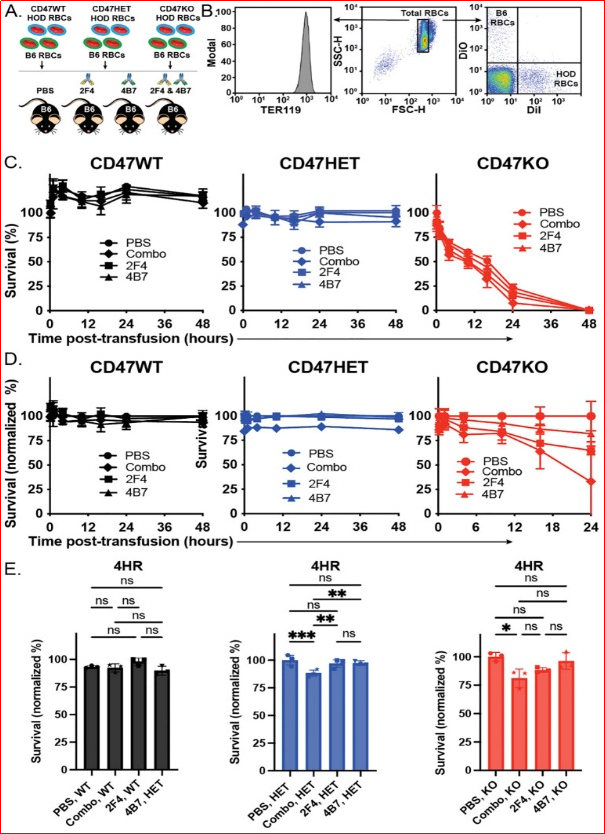
图2. 抗-HEL抗体增强HOD CD47杂合和敲除红细胞的清除,但对HOD CD47 WT红细胞的去除没有影响。
2.3抗-HEL抗体水平在将HOD CD47 WT、杂合和敲除红细胞输注到免疫受体体内后随时间下降。
检测输血后不同时间点的抗体结合情况,在体外与每种单克隆抗-HEL抗体孵育后观察到的抗体结合水平一致,输注后10分钟内,在每个免疫受体中未能检测到抗体结合的显著差异(图3A、D)。与体外孵育时使用单克隆抗-HEL抗体组合相比,每种单克隆抗-HEL抗体单独使用时观察到的抗体结合增强不同,输注到受体中时,使用抗体组合的抗体结合反而减少,而单一单克隆抗-HEL抗体则没有这种现象(图3A、D)。与输血后10分钟的观察结果类似,将每种HOD供体红细胞输注到仅接受单一抗体免疫的受体中时,检测到的抗体水平较高,而将相似的HOD供体红细胞输注到已接受组合型抗-HEL抗体免疫的受体中时,抗体水平较低(图3A-D)。尽管输注后HOD CD47 WT、HOD CD47 HET和HOD CD47 KO红细胞上的抗体水平最初是相似的,但在仅接受单一抗-HEL抗体免疫的受体中,HOD CD47 KO红细胞上的抗体水平下降更为明显,这种结合抗体水平的差异在输血后24小时仍然存在于每个红细胞群体中(图3A-D)。
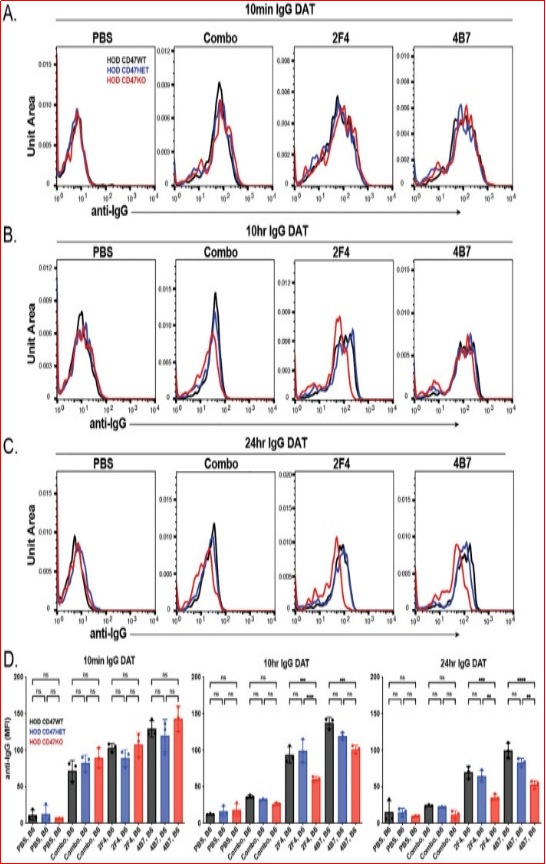
图3. 抗-HEL抗体水平在将HOD CD47 WT、杂合和敲除红细胞输注到免疫受体体内后随时间下降。
2.4抗-HEL抗体降低HOD抗原在HOD CD47 WT、杂合和敲除红细胞上的水平。
在输血后不同时间点分析了受体中的HOD抗原水平,结果表明,在仅接受单一抗-HEL抗体免疫的受体中,输血后不同类型的HOD红细胞(HOD CD47 WT、HOD CD47 HET和HOD CD47 KO)表面的HEL抗原水平没有显著变化(图4A、D)。然而,当每种HOD供体红细胞群体被输注到已接受多种抗-HEL抗体免疫的受体中时,检测到的抗-HEL抗体水平显著下降(图4A、D)。与抗体水平相似,抗原水平在输血后持续下降,且在接受抗-HEL抗体免疫的受体中,抗原检测的下降速度和幅度在使用抗-HEL抗体组合时比单一抗-HEL抗体时更为明显(图4A-D)。这些结果与先前的研究一致,表明抗-HEL抗体的组合在诱导可检测抗原水平下降方面更为有效。
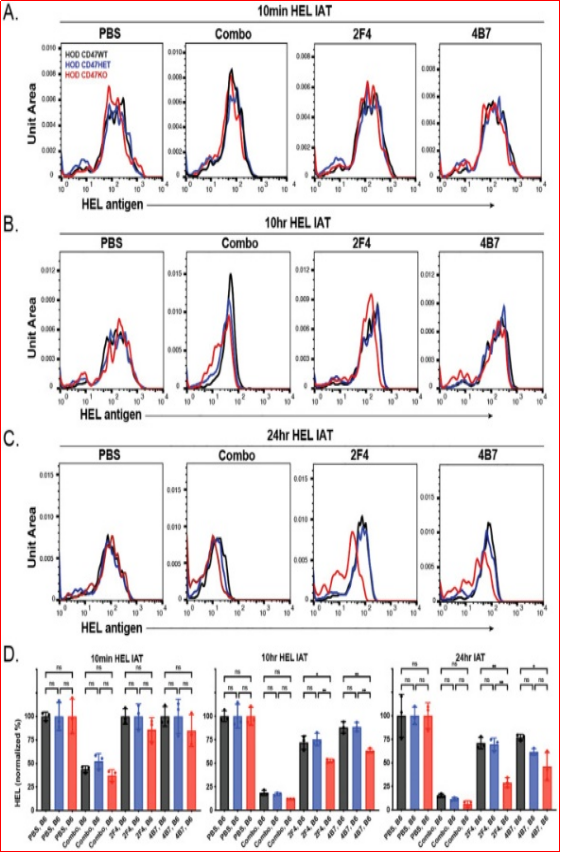
图4. 抗-HEL抗体降低HOD抗原在HOD CD47 WT、杂合和敲除红细胞上的水平。
2.5抗体介导的HOD CD47杂合和敲除红细胞清除增强作用需要Fcγ受体。
为确定观察到的HOD CD47 HET和HOD CD47 KO红细胞在输注到免疫受体后加速清除是否反映了Fcγ受体依赖性或非依赖性过程,将HOD红细胞输注到未免疫或免疫的WT或FcγR KO受体后红细胞的清除情况。由于在接受组合型抗-HEL抗体免疫的受体中,HOD CD47 HET和HOD CD47 KO红细胞的抗体介导的清除差异最为显著,因此使用抗-HEL抗体组合对每个受体进行被动免疫。与将HOD CD47 HET红细胞输注到免疫的WT受体中后观察到的增强清除相比,在免疫的FcγR KO受体中,未观察到类似的抗体介导的清除增加(图5A-D)。同样,将HOD CD47 KO红细胞输注到免疫的FcγR KO受体后,抗体介导的加速清除也未能发生,与WT受体相比,清除效果没有显著差异(图5A-D)。
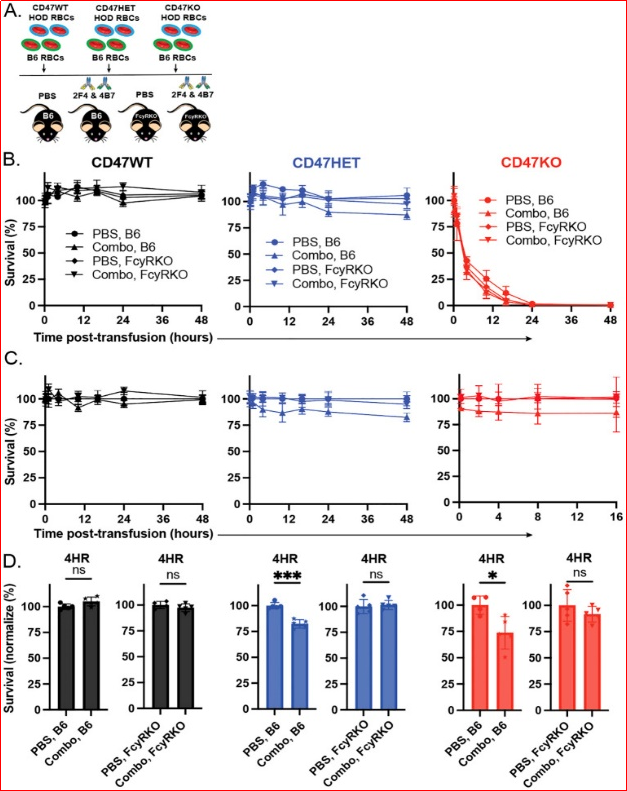
图5. 抗体介导的HOD CD47杂合和敲除红细胞清除增强作用需要Fcγ受体。
2.6抗-HEL抗体结合水平在将HOD CD47 WT、杂合和敲除红细胞输注到WT和Fcγ受体免疫的受体后随时间下降。
为确定在将HOD CD47 WT、HOD CD47 HET和HOD CD47 KO红细胞输注到抗-HEL免疫的WT或FcγR KO受体后,能否观察到抗体结合的差异,本研究检测了红细胞表面的抗体水平。与将每种HOD红细胞群体输注到抗-HEL免疫的WT受体后获得的结果相似,在将这些红细胞群体输注到抗-HEL免疫的FcγR KO受体后,检测到的抗体水平显著下降(图6A-D)。无论是将HOD CD47 WT、HOD CD47 HET,还是HOD CD47 KO红细胞输注到免疫受体中,抗体水平均未观察到差异(图6A-D),这表明清除差异并非反映了相同时间段内抗体水平的变化。
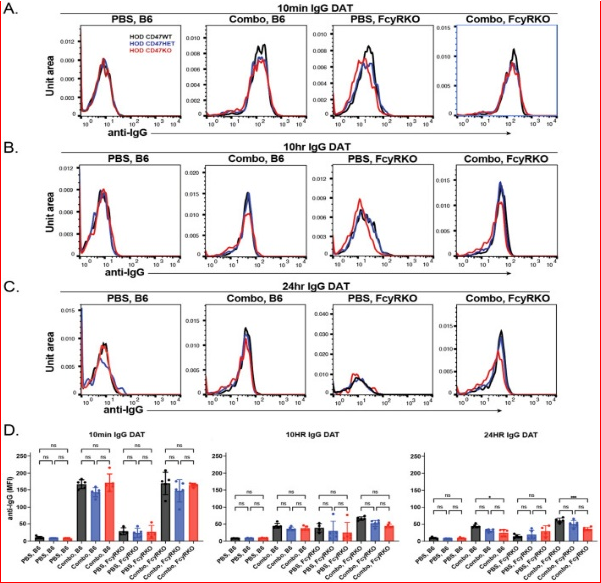
图6. 抗-HEL抗体结合水平在将HOD CD47 WT、杂合和敲除红细胞输注到WT和Fcγ受体免疫受体体内后随时间下降。
2.7抗-HEL抗体降低HOD抗原水平,但不改变Ter119水平或引发补体沉积。
本研究检测了输注后的红细胞表面HOD抗原水平,与输注到每个抗-HEL免疫受体后观察到的抗体水平减少相似,HOD抗原水平在输注到抗-HEL免疫的WT或FcγR KO受体后也相应减少(图7A)。为了确定每种情况下抗原丧失是否特异性地发生在HOD抗原上,我们接下来检测了其他红细胞表面结构是否也出现类似的抗原水平变化。为此,我们检测了Ter119,这是一个常用于区分红细胞与其他细胞群体的标志物。尽管在免疫受体中可检测到的抗体和抗原水平随着时间推移减少,但Ter119水平并未发生类似变化(图7B)。与FcγR在抗体介导的清除中的作用一致,输注HOD CD47 HET和HOD CD47 KO红细胞后,几乎未能观察到明显的补体沉积(图7C)。
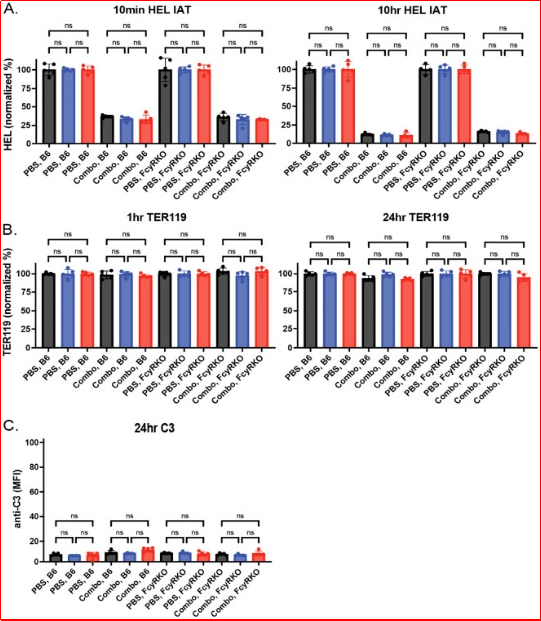
图7. 抗-HEL抗体降低HOD抗原水平,但不改变Ter119水平或引发补体沉积。
3 主要结论
1)CD47在调控红细胞清除和抗体介导的调节过程中起着重要作用,提示CD47可能是调节红细胞在不相容输血后抗体介导清除结果的关键特征。
2)CD47调节抗体结合后红细胞清除的能力可能反映了抗体通过FcγR激活吞噬细胞与CD47-SIRPa在吞噬作用中的抑制效应之间的相互作用。在当前模型中,CD47调节的红细胞循环时间和抗原水平的变化被认为是诱导异体免疫反应的关键因素。
3)该研究发现抗体能够诱导抗原调节,在无法获得完全相容红细胞的情况下,利用这一结果可能有助于增强靶抗原的变化,从而优先调节抗原,而不是单纯依赖红细胞的清除。
4 文献来源
Ryan P Jajosky, Mischa L Covington, Jun Liu, et al. CD47 regulates antigen modulation and red blood cell clearance following an incompatible transfusion. Front Immunol.2025:16:1548548.doi: 10.3389/fimmu.2025.1548548.
全文审校:李志强 潘 健