国际输血医学最新动态2025年第12期
血浆细胞外囊泡研究新进展
前言
本期《国际输血医学新进展》聚焦于血浆细胞外囊泡(EVs)的功能、不同分离方法各自优缺点及临床应用潜力。研究者们评价了不同分离方法的优缺点,发现单次冻融处理对EVs完整性、形态及蛋白质组成无显著影响,为生物样本库建立和大规模EVs研究提供了重要参考。单纯的EVs分离方法结合质谱与聚类/机器学习,在复杂样本中精准解析EVs蛋白质组,为疾病诊断提供实用新路径。揭示了血浆EVs作为系统性免疫稳态调节器的双重通路机制,促进中性粒细胞-巨噬细胞相互作用,加速炎症消退。这些研究成果强调了根据研究目标选择合适分离技术的重要性,为未来多种疾病的诊断及后续治疗提供了新的思路和见解。
血浆细胞外囊泡表面定位的GAS6/PROS1和CD39/CD73可减轻炎症反应
编译者:张婧,陈要臻;审校:尹文
研究背景
炎症是一种保护性反应,有助于清除有害刺激物(如入侵病原体)。该过程涉及血管变化,促进白细胞和血浆成分向损伤部位的快速招募。巨噬细胞与中性粒细胞共同通过非氧化性(即杀菌酶)及NADPH依赖性氧化杀菌机制,对入侵病原体实施吞噬杀灭。中性粒细胞和巨噬细胞还可分泌多种细胞因子和趋化因子,进一步诱导血管变化并招募更多细胞。然而,巨噬细胞和中性粒细胞的活性需要受到精确调控,以避免炎症反应持续和组织损伤。多种活性机制共同参与终止炎症信号并恢复组织稳态。细胞外囊泡(EVs)是富含蛋白质的纳米级结构,由脂质包膜包裹。EVs由细胞释放,存在于包括血液在内的所有体液中。与靶细胞相互作用时,EVs可通过释放其内容物或通过表面分子刺激细胞受体。由于炎症组织中内皮细胞形成渗漏间隙,血液中的外泌体得以进入并在此类区域积聚,从而促进其与细胞的相互作用。本研究发现血浆外泌体中存在表达磷脂酰丝氨酸(PS)的亚群,这些外泌体可被GAS6和/或PROS1修饰,从而激活巨噬细胞受体,进而诱导巨噬细胞呈现促炎表型。同时,位于EVs表面的CD39和CD73可通过促进ATP水解和腺苷生成来调节中性粒细胞活性。本研究揭示了血浆EVs作为系统性免疫稳态调节器调节炎症反应的全新机制。
主要结果
1.巨噬细胞
作者近期报道了外泌体能抑制巨噬细胞的炎症反应,据此提出假说:外泌体冠层中存在抗炎性TAM受体配体蛋白GAS6和PROS1。从健康人血浆中分离的EVs高表达膜相关蛋白(CD63、CD81和CD9)及胞质蛋白(Alix、HSP70、syntenin-1和flotilin-1),低表达高密度脂蛋白(HDL)和低密度脂蛋白(LDL)标志物APOA1与APOB100(图1A、1B)。透射电子显微镜(TEM)分析显示分离的EVs具有正常形态(图1D)。纳米流式细胞术(NFCM)分析揭示EVs平均直径为76.49 nm(±SD 4.10 nm)(图1E)。研究发现约21%的血浆EVs表面镶嵌着GAS6/PROS1蛋白(图1K-1M),这些蛋白就像"分子桥":一端通过PS锚定在EVs上,另一端激活巨噬细胞表面的MERTK受体。激活后的MERTK会触发三重抗炎效应:启动SOCS1/3信号通路(抑制炎症的"刹车蛋白"),降低促炎因子IL-6(从300pg/mL降至50pg/mL),并提升抗炎因子IL-10(升高约3倍)(图2)。当用维生素K拮抗剂处理时,EVs失去这种调节能力(图1N),证实该机制依赖维生素K修饰的蛋白结构。
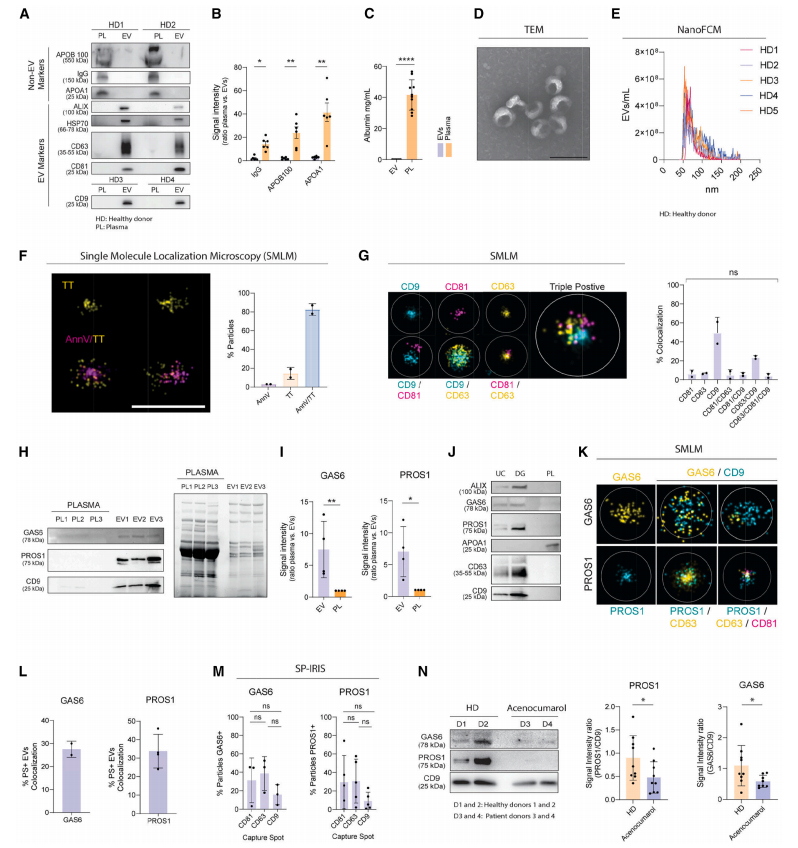
图1. 人血浆细胞外囊泡中的一部分表面有TAM受体配体GAS6和PROS1
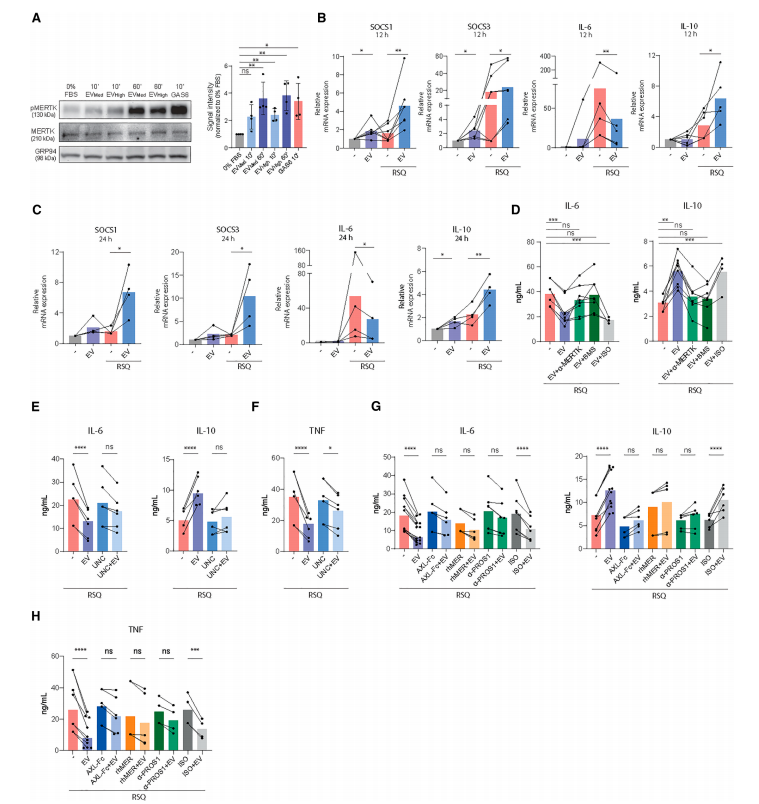
图2. TAM受体信号传导对EV抑制巨噬细胞活性至关重要
2. 中性粒细胞
鉴于大量研究强调细胞外腺苷在中性粒细胞活化调控中的重要性,且血浆外泌体携带能生成细胞外腺苷的酶,作者据此提出假说:外泌体通过促进炎症性细胞外ATP水解为抗炎性细胞外腺苷来调节中性粒细胞活化。作者首先分析纯化外泌体中这些酶的存在情况。检测到CD39(胞外核苷三磷酸二磷酸水解酶-1,可水解ATP生成ADP,继而生成AMP)和CD73(胞外5'-核苷酸酶,可水解AMP生成腺苷)存在于外泌体中(图3A-3B)。流式细胞术分析证实,血浆EVs表面携带CD39和/或CD73的占比为21.33%(图3C),它们能将促炎信号ATP(三磷酸腺苷)逐步降解为抗炎物质腺苷:ATP → ADP → AMP → 腺苷。这个"分子加工厂"效率惊人:1 μM ATP在30分钟内被降解80%(图3D)。产生的腺苷通过A2A受体抑制中性粒细胞:减少活性氧产生(降低40-60%),抑制颗粒释放(CD66b表达下降35%),促进TGF-β分泌(增加2倍)。更有趣的是,被EVs修饰的中性粒细胞会主动寻找巨噬细胞。共培养实验显示:细胞结合率提高50%,促进巨噬细胞释放IL-10(升高2.5倍),抑制IL-6产生(降低60%)(图4)。这种"三方会谈"机制解释了炎症消退时免疫细胞如何协同工作。
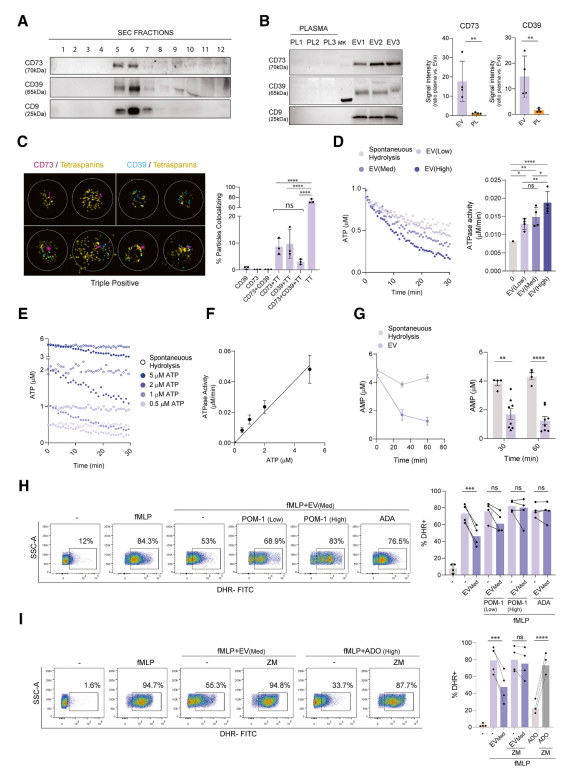
图3. CD39/CD73/腺苷通路参与抑制EV依赖性中性粒细胞氧化爆发
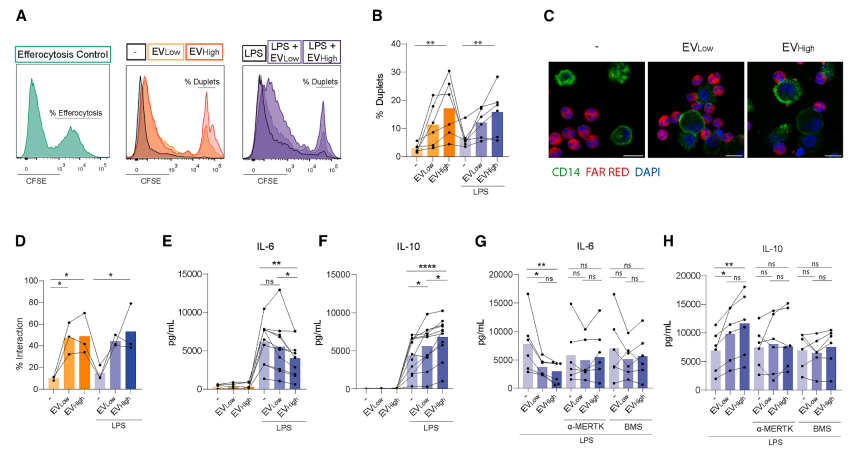
图4. EV处理的中性粒细胞诱导巨噬细胞样单核细胞呈现抗炎表型
主要结论
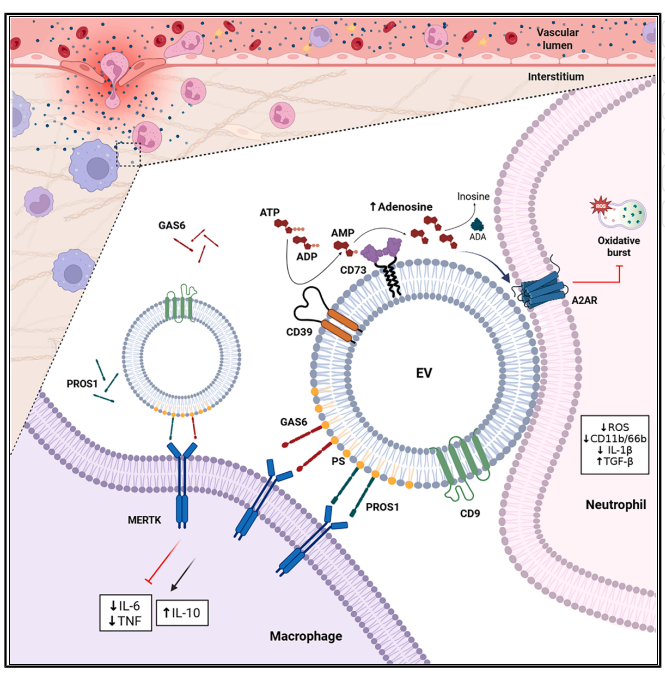
健康人血浆中的细胞外囊泡(EVs)通过两种独立机制调控先天免疫。(1)巨噬细胞调控:依赖GAS6/PROS1-MERTK信号通路,EVs表面携带的GAS6/PROS1通过结合巨噬细胞MERTK受体,上调SOCS1/3,抑制IL-1β/IL-6,促进IL-10/TGF-β分泌。(2)中性粒细胞调控:依赖CD39/CD73-腺苷通路,EVs表面的CD39/CD73将促炎性ATP降解为抗炎性腺苷,通过A2A受体抑制中性粒细胞ROS爆发和脱颗粒。EVs促进中性粒细胞-巨噬细胞相互作用,加速炎症消退。这项研究揭示了血浆EVs作为系统性免疫稳态调节器的双重通路机制,为多种疾病治疗提供新思路。
文献来源
Fabiano MP, Adamczyk AM, Gololobova OA, Mazzitelli IG, Leicaj ML, Grosso TM, Pérez PS, Alvarez CL, Schachter J, Palmer S, Sabbione F, Erra Díaz FA, Trevani AS, Varas-Godoy M, Carrera Silva EA, Witwer KW, Ostrowski M. Plasma extracellular vesicle surface-located GAS6/PROS1 and CD39/CD73 attenuate inflammation. Cell Rep. 2025 Aug 26;44(8):116096. doi: 10.1016/j.celrep.2025.116096. Epub 2025 Aug 2. PMID: 40751911.
系统评估分离技术及冻融效应对血浆细胞外囊泡异质性与亚群普分析的影响
编译:樊晗璐,陈要臻; 审核:尹文
研究背景
细胞外囊泡(EVs)是微小的膜结合颗粒,通过转移DNA、RNA、蛋白质和脂质等多种生物分子,在细胞间通信中发挥关键作用。血液来源的外泌体(EVs),尤其是血浆外泌体,因其易于获取且含有来自不同组织、器官和细胞类型的多种生物分子,在精准医学领域具有巨大潜力。研究证实血浆外泌体携带的分子生物标志物可辅助多种病理状况的疾病诊断、治疗反应分层及预后评估。此外,特定血浆EV亚群已被证实与阿尔茨海默病及结直肠癌的早期发展相关。EVs被公认为极具潜力的疾病生物标志物和治疗载体。然而,由于EV群体异质性及分离技术的差异性,标准化血液来源EV的分离仍具挑战性。本研究系统地评估了三种不同的EV分离方法:不对称流场流分馏法(AF4)、尺寸排阻色谱法(SEC)以及结合功能化膜的自动化离心微流盘系统(Exo-CMDS),从多个层面为血浆EVs分离方法的选择和标准化提供了综合性的系统评价。
主要结果
1. 分离EVs颗粒的形态与粒径分布
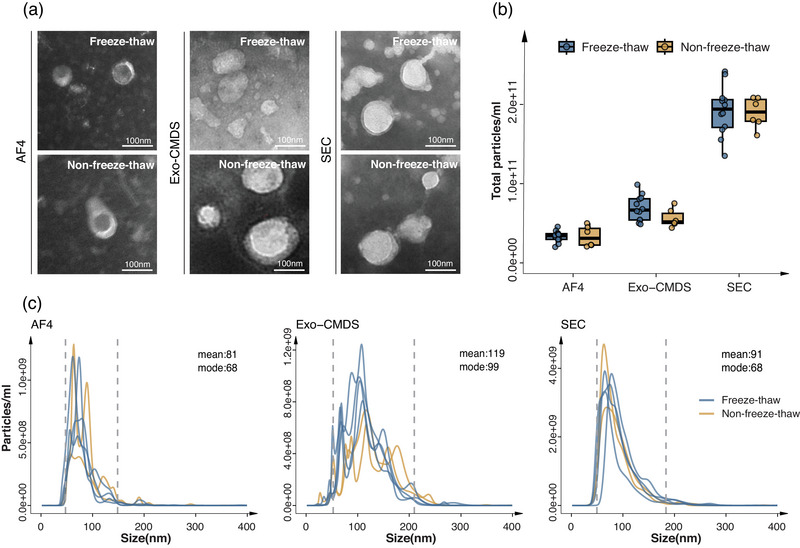
通过对三种分离方法所得EVs透射电子显微镜(TEM)验证以及纳米粒体分析(NTA),结果显示三种分离方法均有典型的EV形态;SEC分离的EVs产量显著最高,其次为Exo-CMDS分离样本,而AF4样本的颗粒产量最低。AF4分离的EV粒径分布相对狭窄(50-130 nm),SEC分离的EV粒径分布处于中间范围(50-160 nm)(图2c)。而Exo-CMDS分离的EV粒径分布最宽(50-190 nm)。在三种EV分离方法中,经冷冻-解冻处理与未经处理的样本间未观察到显著的颗粒浓度差异,表明单次冷冻-解冻循环对EV产率影响甚微。
2. 基于PBA的单电子伏特表面蛋白质组谱分析
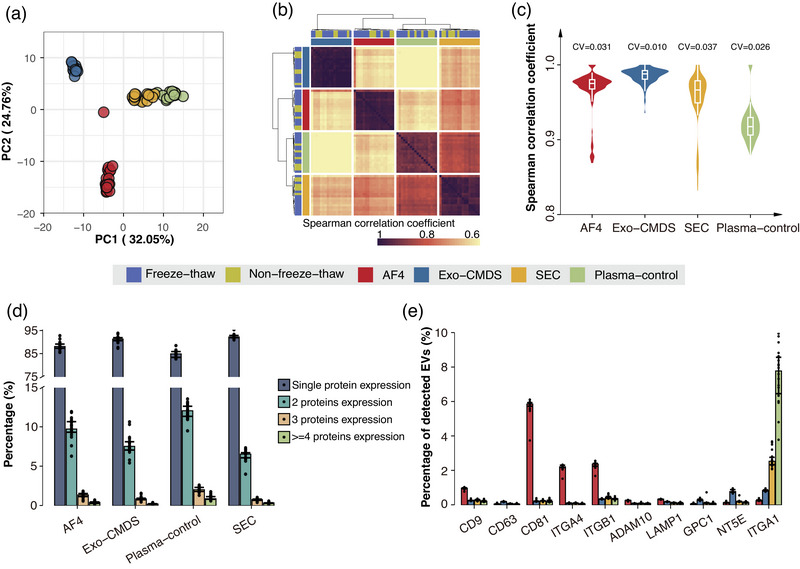
为系统性研究外泌体群体的组成,研究者采用基于PBA的单外泌体表面蛋白组测定法,分析了通过AF4、Exo-CMDS和SEC三种不同分离技术从18份血浆样本中分离的外泌体。结果显示AF4分离的EVs富集经典跨膜蛋白亚群(CD151、CD81、CD9等),Exo-CMDS分离的EVs富集免疫相关蛋白亚群(CD5、NT5E、TNFRSF9、ITGB2),SEC分离的EVs富集ESC偏好的EVs亚群(THBD、SELL、CDH12等)。
3. 不同分离方法EV亚群的变异性
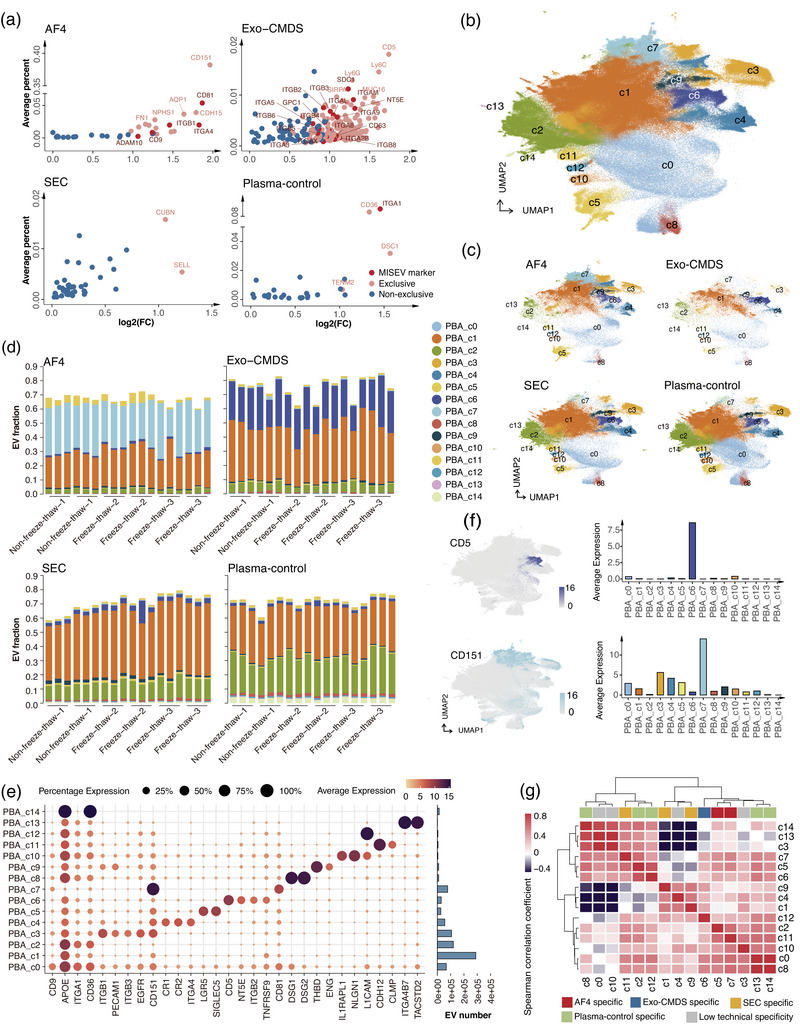
研究者通过检测仅表达单一表面蛋白或多重表面蛋白的外泌体,研究了技术特异性外泌体亚群。对于检测到单一表面蛋白的EVs,研究者采用方差分析(ANOVA)比较其在所有组别中的丰度分布。该分析识别出35种富集于AF4组的单蛋白EVs、229种富集于Exo-CMDS组、42种富集于SEC组以及28种富集于血浆对照组。在这些单蛋白EV中,17种在AF4组富集最高,167种在Exo-CMDS组,2种在SEC组,5种在血浆对照组。UMAP分布图显示新鲜血浆分离的EVs与SEC分离的EVs高度重叠,说明SEC分离的EVs与新鲜血浆分离的EVs表面蛋白亚群构成几乎一致。
4. 基于液相色谱-质谱联用技术的外泌体蛋白组谱分析
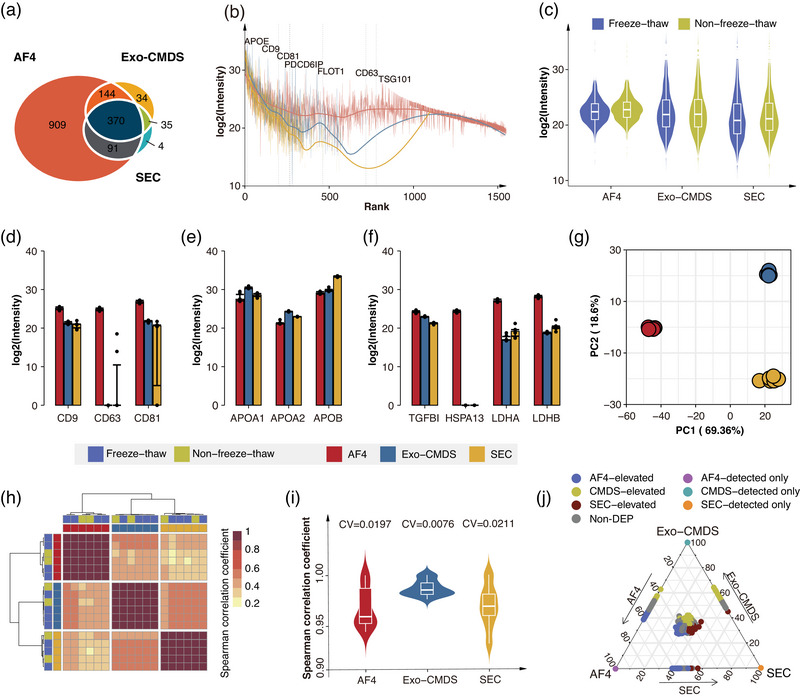
研究者采用LC-MS/MS技术对整个EV蛋白组进行定量分析。所有样本共定量出1588种蛋白。后续分析聚焦于每种技术组中至少60%样本检测到的蛋白质。最终获得AF4组1514种蛋白质、Exo-CMDS组583种蛋白质及SEC组500种蛋白质。这三组样本共同检出370种蛋白质。
4. EV蛋白质组谱的聚类分析与功能注释
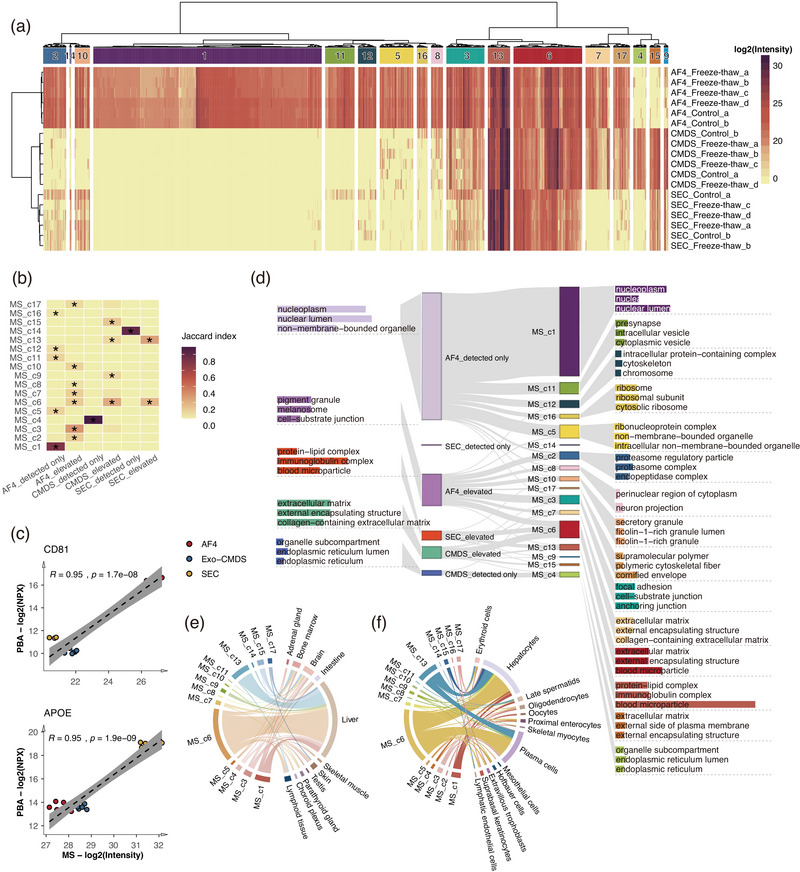
为深入解析这些技术特异性外泌体蛋白的共表达模式及其功能意义,研究者们对通过LC-MS/MS定量分析的1588种蛋白质进行了层次聚类分析,最终识别出17个独立蛋白质簇。AF4富集核源性组分、细胞-基质连接蛋白及蛋白酶体相关蛋白;Exo-CMDS富集内质网、高尔基体及细胞外基质相关蛋白,同时富含血小板颗粒标记蛋白的EVs;SEC富集蛋白-脂肪复合物和免疫球蛋白复合物。单次冷冻-解冻对EVs的蛋白普和亚群分布均无显著影响。Exo-CMDS和SEC高表达蛋白以及三种分离方式共同表达的蛋白簇主要来源于肝脏。
主要结论
本研究结合透射电子显微镜(TEM)、纳米颗粒追踪分析(NTA)、单个外泌体表面蛋白组学及整体蛋白组学分析,探讨了通过AF4、E-CMDS和SEC技术分离外泌体的优势与局限性。AF4分离所得EVs纯度高,粒径分布较均一,蛋白覆盖度最广。SEC产率最高,但伴随脂蛋白等非囊泡成分共分离。Exo-CMDS产率中等,富集免疫相关亚群。研究者们还发现单次冻融处理对EV完整性、形态及蛋白质组成无显著影响,为生物样本库建立和大规模EV研究提供了重要参考。这些发现强调了根据研究目标选择合适分离技术的重要性。
文献来源
Xueqi Li, Xiangyu Li, Lingjun Tong, Liqiao Hu, Yanfen Hong, Ruoyu Zhou, Zonghong Li, Ming Dong, Junjie Hou, Tao Xu, Wen Zhong. Systematic Evaluation of Isolation Techniques and Freeze-Thaw Effects on Plasma Extracellular Vesicle Heterogeneity and Subpopulation Profiling. J Extracell Biol. 2025 Jun 26;4(6):e70058. doi: 10.1002/jex2.70058. PMID: 40575388.
血浆外泌体生物标志物开发的前沿蛋白质组学
分析中的挑战与机遇
编译:徐金梅,陈要臻;审核:尹文
研究背景
细胞外囊泡,包括外泌体,因其具有免疫中性、能够跨越生物屏障、并能递送多种类型货物(包括转基因、RNA、DNA和功能性蛋白质)的特性,正在成为疾病诊断及治疗的新兴载体。在众多囊泡中,血浆衍生的细胞外囊泡 (pEVs) 由于血浆在全身循环,它几乎可以从所有组织和器官中收集囊泡,尤其令人兴奋。这意味着,只需一次简单、微创的抽血,一份血浆样本就能为了解全身健康状况打开一扇窗户,而静脉囊泡输注则可能实现全面治疗的目标。
pEVs蛋白质组学是研究血浆中细胞外囊泡(如外泌体、微囊泡等)所携带蛋白质的组成、结构、功能及动态变化的学科领域,具有重要的临床应用价值。但血浆中富含与pEVs理化性质相似的脂蛋白、蛋白聚集体等干扰成分,常导致 EVs 纯化难以兼顾纯度与回收率,且操作繁琐、可重复性低,从pEVs中提取蛋白信息具有极大挑战性。而富集pEVs的技术各有优缺点,没有一种能够将pEVs纯化至完全均一。因此富集方法成为pEVs生物标志物开发的核心问题。
在对pEVs的组成进行更好的表征后提出的在复杂样本中定量pEVs蛋白,即结合蛋白质谱对pEVs进行定标定量可能是开发生物标志物的更可行路径。这样即使样本中存在杂质,质谱仪仍可提供对pEVs蛋白组的可重复深度覆盖。
设计思路
1. 纯化pEVs:依据 6 类pEVs分离方法的核心特点 —— 离心法(易操作但伤pEVs)、SEC(温和回收率高但混脂蛋白)、免疫亲和法(特异性富集但成本高)、电荷基 Mag-Net 法(仅需 100μL 血浆适配高通量)、AF4(高分辨率但需优化流速)、多模态色谱法(减少样本损失但脂蛋白去除有限),评估各类方法的难易程度实现微量高纯度pEVs的获取方法。
2. 蛋白质组学分析:在质谱技术中,将DDA/DIA 用于非靶向发现与验证,SRM/PRM 用于靶向定量,通过机器学习(如 LASSO、混合算法)筛选标志物、构建诊断模型。从概念上讲,混合型 DIA 质谱采集策略非常有前景,因为它结合了无偏倚的基于 DIA 的分析与假设驱动的定量,同时在单次运行中提供提高通量和覆盖范围的优势。
整合先进生物信息学工具以优化pEVs蛋白组图谱、识别新型生物标志物以及简化生物标志物开发验证流程提供了机会。通过专注于利用技术而非追求绝对纯度,这一方法能够改变现有实践并为稳健的生物标志物发现开辟新天地。
结论示意
1. EVs 作为疾病生物标志物示意图
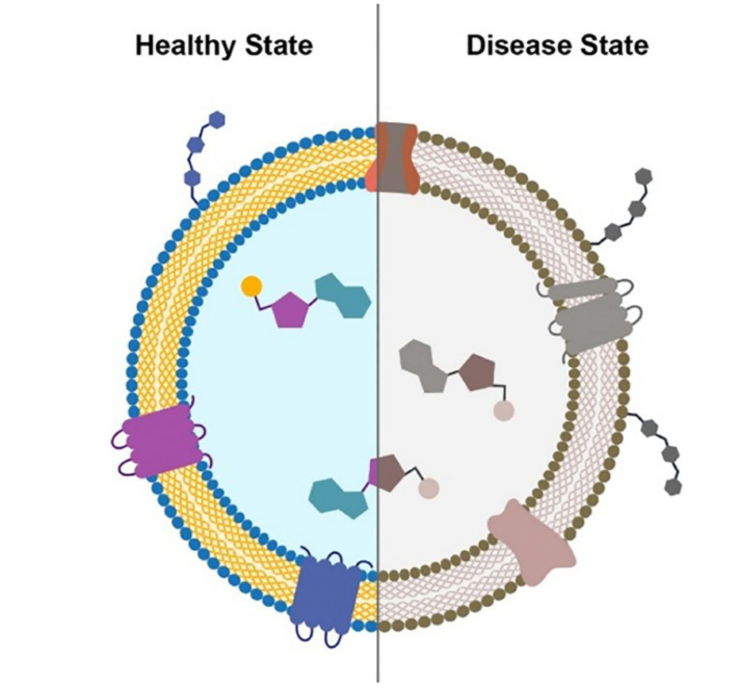
图 1
健康状态下 EVs 携带正常蛋白(如 CD9/CD63),疾病状态下新增病理相关蛋白(如帕金森病 α- 突触核蛋白),明确 EVs 蛋白组成的 “状态依赖性” 是其作为标志物的基础。
2. EVs 纯化方法对比
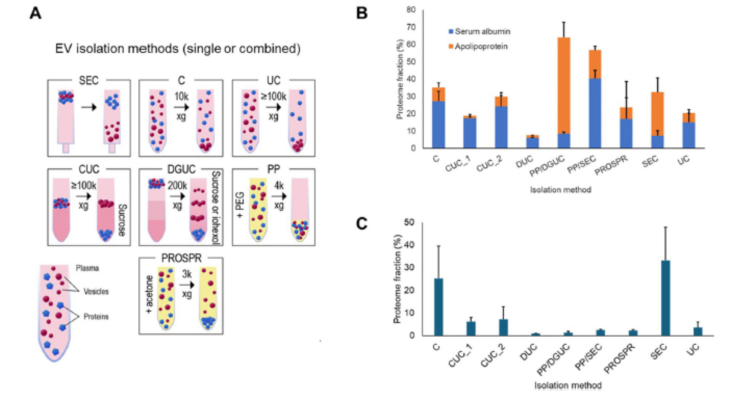
用于蛋白质组学分析的外泌体(EV)纯化方法。(A) 使用不同的方法分离血浆外泌体。(B) 不同纯化方法下常见外泌体制备污染物的丰度。(C) 不同纯化方法下富集EV蛋白组的丰度。证实 SEC 在去污染与保回收间平衡最优。
3. 血浆EV蛋白组聚类分析
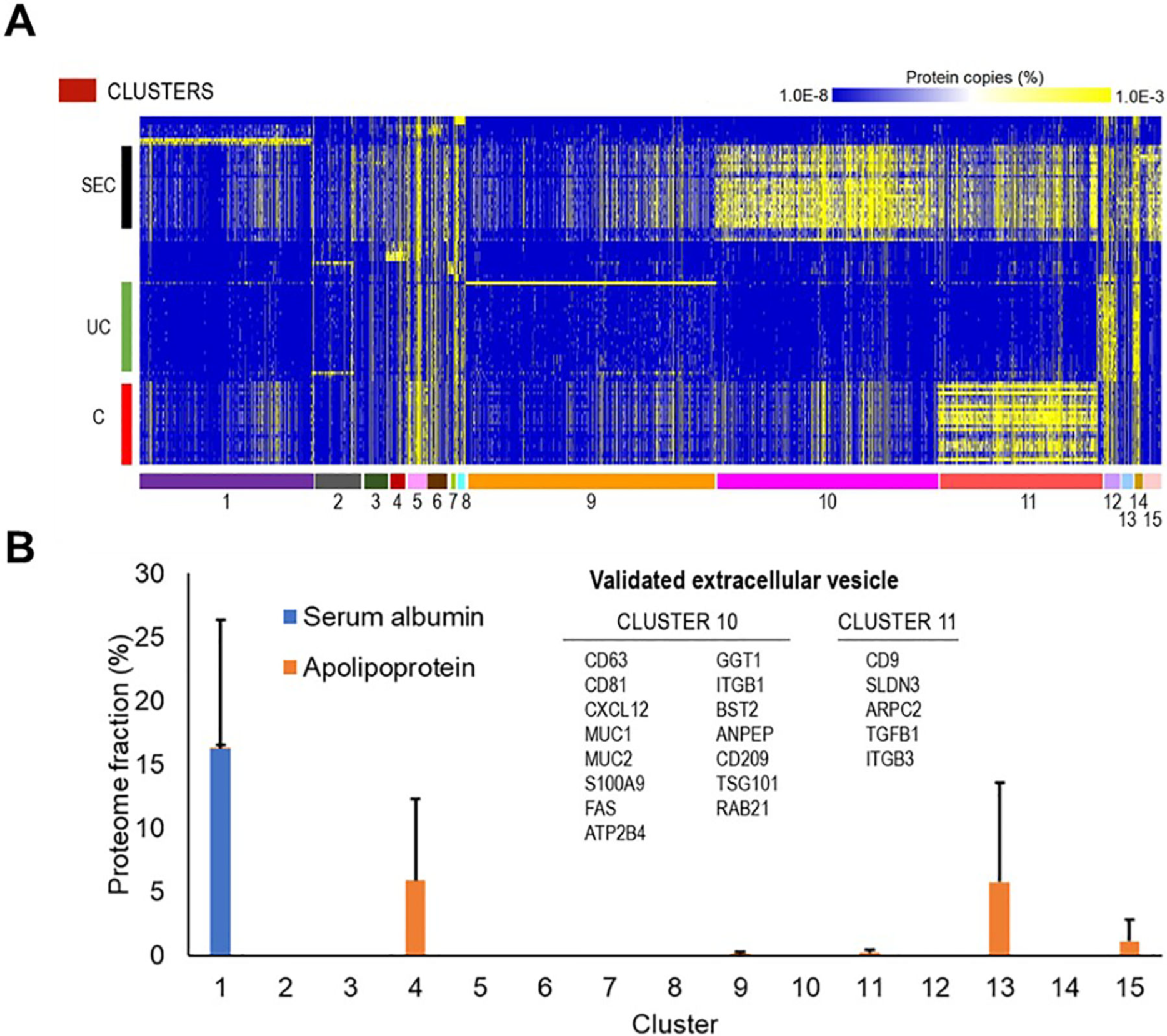
(A) 使用Vesiclepedia中排名前100的EV蛋白的最高富集簇。 (B) 蛋白组元分析中不同簇的常见细胞外囊泡制备污染物丰度。提出 “聚类分析区分 EV 蛋白与污染物” 的新策略。
4. 质谱分析 EV 蛋白质组思路图
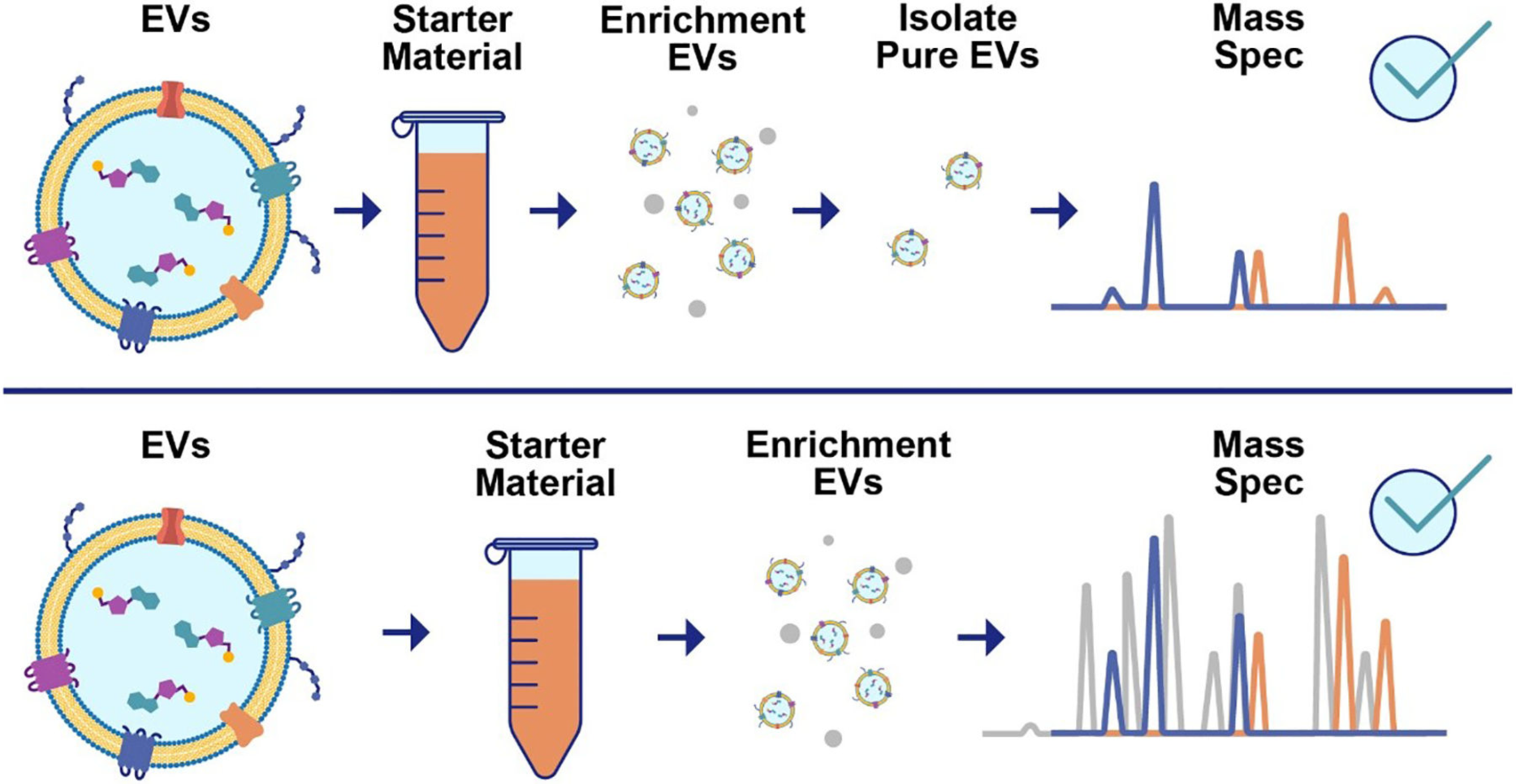
对比传统 “富集→纯化纯 EVs→质谱”(损失大、需大样本)与新路径 “富集→直接质谱”(高灵敏检测、适配小样本),突出新路径更适合大规模标志物筛选。
全文总结
综上所述,以往认为的获取纯净的pEVs制备物是基于pEVs成分的生物标志物开发过程中的重大挑战。但由于需要大量样本和多重纯化步骤,纯净的EV制备物可能不适合生物标志物研究。那么这种新的概念:更好地表征pEVs组成,然后在富集但仍然复杂的样本中进行深度蛋白质组学分析,可能是一种更可行的替代方法。虽面临基于图像的高通量方法来验证蛋白质在囊泡中的定位、小样本回收待提升等问题,但未来自动化富集、单pEVs技术及临床多中心验证,将推动pEVs标志物从实验室走向临床,为疾病诊断提供实用新路径。
文献来源:Dakup PP, Ludovico ID, You Y, Rao C, Flores J, Bramer LM, Rewers M, Webb-Robertson BM, Metz TO, Mirmira RG, Sims EK, Nakayasu ES. Challenges and Opportunities in State-of-the-Art Proteomics Analysis for Biomarker Development From Plasma Extracellular Vesicles. Proteomics. 2025 Sep 16:e70036. doi: 10.1002/pmic.70036. Epub ahead of print. PMID: 40955644; PMCID: PMC12604859.