红细胞外囊泡的研究现状
本期《输血医学新进展》聚焦于红细胞来源细胞外囊泡(REVs)在生理稳态维护与精准载药递送领域的最新研究突破。通过分析三篇前沿文献,内容涵盖了红细胞外囊泡在皮肤与毛发稳态中的生理功能、工程化REVs协同递送化疗药物与基因药物以强化白血病靶向治疗,以及利用REVs递送siRNA靶向骨骼肌以干预癌症恶病质的新策略。相关研究不仅系统展示了红细胞来源囊泡作为天然生物载体在跨组织递送及复杂疾病联合治疗中的巨大潜力,也为拓展红细胞的功能研究与临床应用转化提供了创新的理论支撑与实践参考。
红细胞外囊泡融入毛发与皮肤以维持稳态
编译者:曾媛 审校者:黄远帅
背景
红细胞是人体循环系统中数量最多的细胞,约占人体细胞总数的70%,具有向全身组织运输氧气、向肺部排出二氧化碳,维持一氧化氮稳态、氧化还原平衡、免疫调节及凝血功能等多种重要作用。由于成熟红细胞不具备细胞核及线粒体、核糖体等细胞器,因此可将其视为富含血红蛋白的高度特异化大型细胞外囊泡(EVs)。器官系统通过协同作用完成复杂功能以维持正常生理活动,包括皮肤、指甲、毛发及体表腺体的表皮系统是抵御病原体侵入、穿透性物体及紫外线辐射的关键物理屏障。器官系统通过多种生物通路进行沟通,细胞外囊泡可作为载体在器官间传递物质。贫血患者常伴随红细胞数量减少,普遍出现皮肤苍白、干燥粗糙、毛发受损及脱发等问题,因此推测红细胞与表皮系统存在密切关联,但二者相互作用的具体机制尚未明确。雄激素性脱发(AGA)是临床常见的脱发类型,患病率高,目前仅5-α还原酶抑制剂和米诺地尔两种治疗手段,更有效、便捷的疗法有待开发。本研究聚焦红细胞来源外囊泡(EVs),探究其在表皮系统中的作用及相关机制,为毛发再生治疗提供新思路。
主要研究结果
1.贫血小鼠表现出明显的毛发和皮肤损伤:通过乙酰苯肼(APH)诱导建立慢性贫血小鼠模型,发现贫血小鼠不仅红细胞和血红蛋白水平显著降低,还出现毛发无光泽,背部、腹部毛发灰白化、毛发角质层出现裂纹损伤,以及表皮变薄、角质形成细胞核固缩、成纤维细胞数量减少等皮肤毛发组织损伤,证实慢性贫血会严重破坏表皮系统的生理结构与功能。
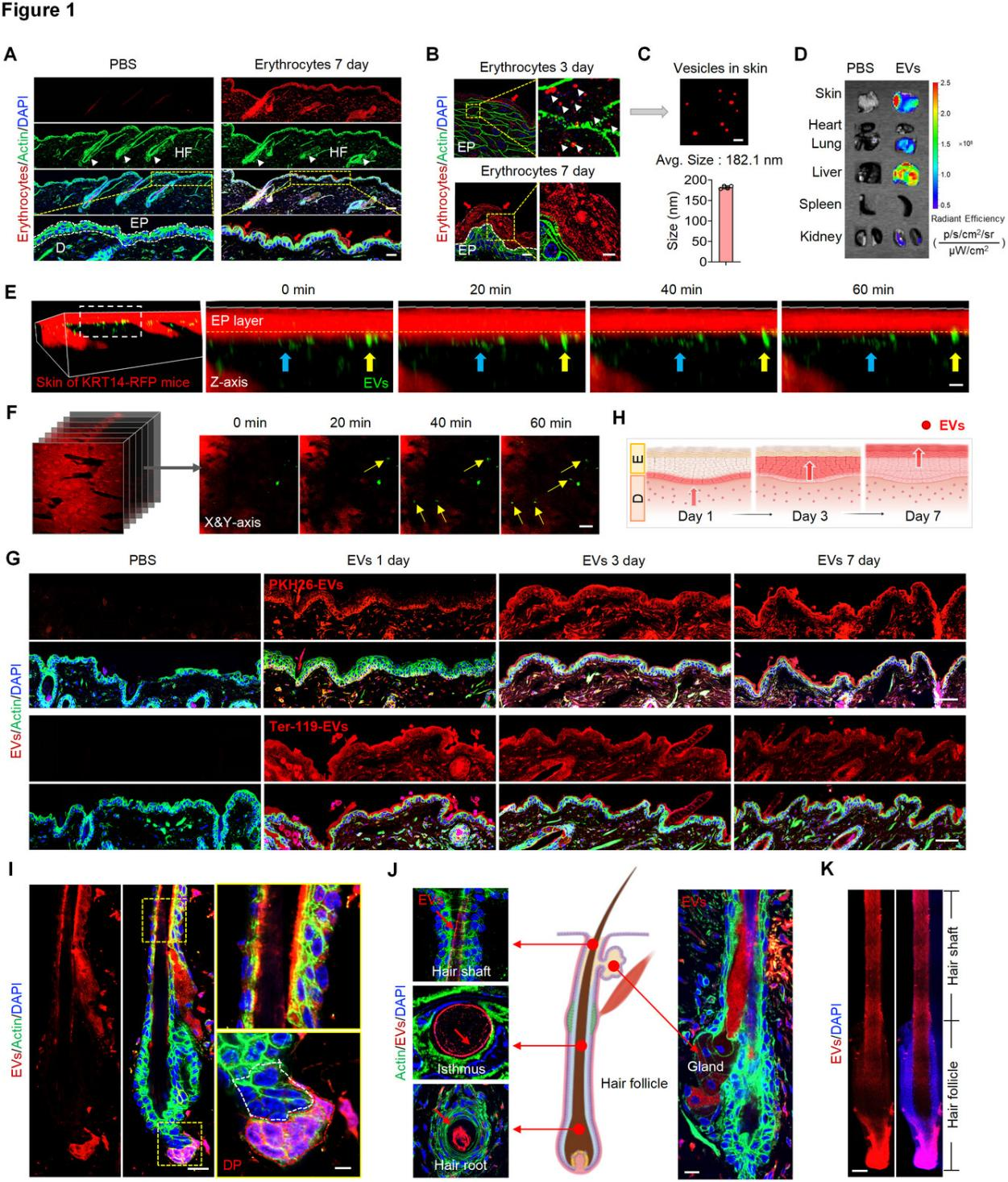
2. 红细胞与红细胞外囊泡在毛发和皮肤的迁移:利用荧光标记和活体成像技术辅助观察,发现小鼠尾静脉注射红细胞后通过血液循环到达表皮层、毛发与毛囊中(图1 D),表明皮肤和毛发是红细胞的主要排泄部位之一。在尾静脉注射PKH26标记的红细胞代谢物后,于表皮层提取出的PKH26阳性颗粒在结构光照明显微镜(SIM)下观察到的囊泡样结构(图1 A-C)。利用纳米流式细胞术(NanoFCM)测定证实其为细胞外囊泡(EVs)。而在活体荧光显微镜(IVIM)记录下,可观察到PKH67标记的红细胞外囊泡在小鼠表皮层中动态移动(图1 E-H);并在注射7天后可观察到小鼠毛囊进入生长期,大量红细胞外囊泡被毛乳头摄取;此外还发现其在皮脂腺中富集,并整合到毛干和毛根中(图1 I-K),表明红细胞外囊泡参与了毛干结构的形成,而红细胞可转化为毛发、皮肤成分。
|
图1 红细胞外囊泡在表皮毛发和皮肤中的生物分布图谱
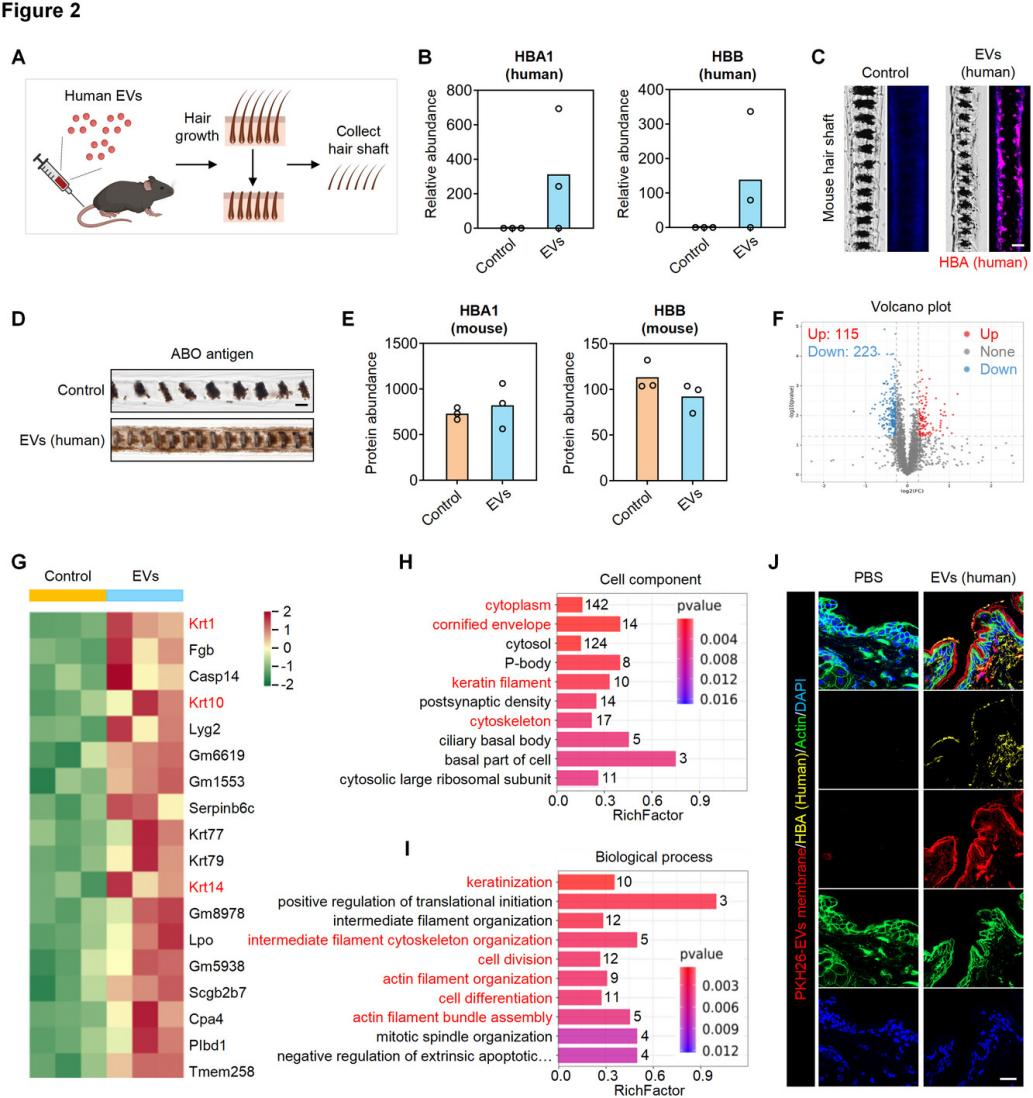
3. 红细胞外囊泡转化为毛发和皮肤成分:蛋白质组学分析显示,静脉注射人红细胞外囊泡后,小鼠毛发中出现人源血红蛋白亚基(HBA1、HBB)和ABO血型抗原(图2 B-E);小鼠自身毛发中的角蛋白(Krt1、Krt10、Krt14等)表达上调(图2 F-I),这些蛋白参与毛发的生长和角质化等生物过程;而7天后,小鼠皮肤中的大部分血红蛋白A(HBA)则留在真皮层,表明红细胞外囊泡可能在皮肤中发生解体,并重新组装成皮肤的不同成分(图2 J)。
|
图2 红细胞外囊泡转化为毛发成分
4. 红细胞外囊泡参与皮肤脂质屏障形成:脂质组学分析表明,红细胞外囊泡富含神经酰胺(Cer)、磷脂酰乙醇胺(PE)、磷脂酰胆碱(PC)和甘油三脂(TG)等脂质;注射红细胞外囊泡后小鼠皮肤表面总脂质含量增加,尤其是表皮屏障重要组成成分神经酰胺、游离脂肪酸、PE等含量上升,且其脂质组成与天然皮脂膜相似,提示红细胞外囊泡可整合至皮肤的表皮结构中。
5. 红细胞外囊泡促进毛发再生的机制:通过测试红细胞外囊泡对C5BL/6和Balb/c小鼠毛发再生的影响发现红细胞外囊泡组小鼠背部皮肤完全被新毛发覆盖,且新生成的毛发远长于5%米诺地尔组(阳性对照)和PBS组(阴性对照)(图3 A-C)。蛋白免疫印迹分析结果显示红细胞外囊泡通过激活真皮毛乳头细胞(DPCs)中Wnt-βcatenin信号通路促进毛发再生的机制(图4 A);进一步对miRNA的研究发现红细胞外囊泡通过miR-20a-5p和miR-22-3p靶向抑制Axin2表达,介导激活Wnt/β-catenin信号通路,从而增强了贫血性骨髓间充质干细胞(SMSC)的增殖率及其成骨、成脂分化能力(图4 C-H)。

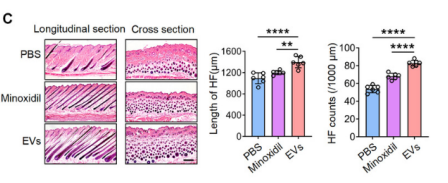
图3 红细胞外囊泡促进野生型小鼠毛发再生,并改善贫血小鼠的毛发和皮肤缺陷。
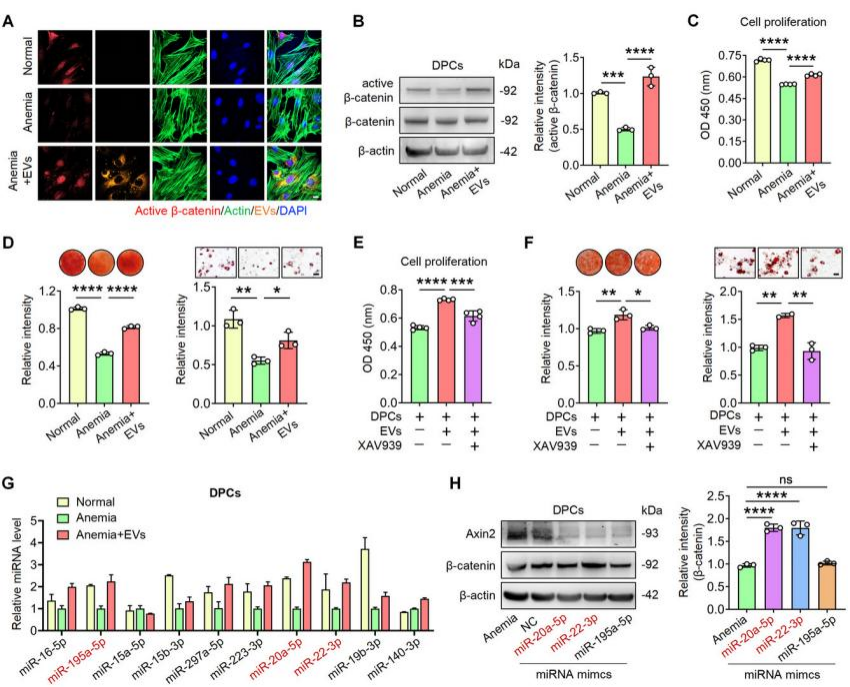
图4 miR-20a-5p和miR-22-3p参与红细胞外囊泡介导的贫血性造血干细胞功能恢复。
6. 临床应用效果:对9名雄激素性脱发(AGA)患者进行3次自体红细胞外囊泡局部注射治疗及6个月随访,结果显示患者生长期头发比例、头发密度和毳毛密度均显著提高,证实自体红细胞外囊泡可有效改善AGA患者毛发生长状况(图5)。
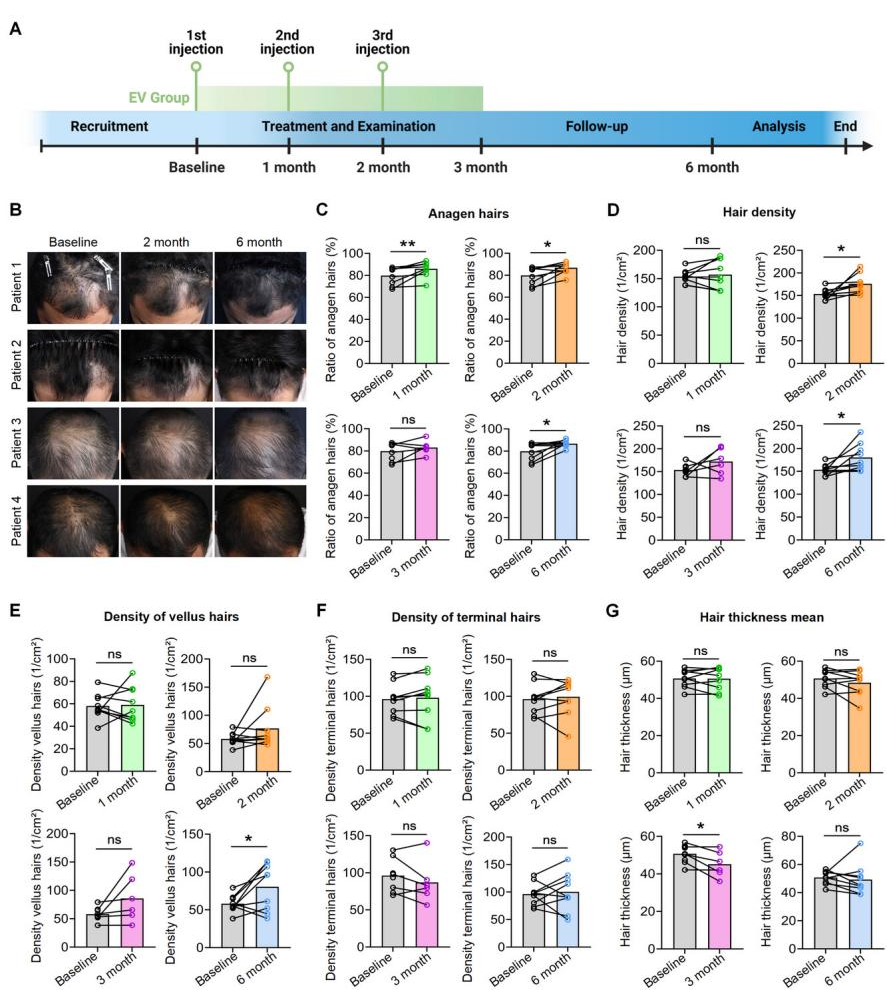
图5 红细胞外囊泡促进AGA患者毛发再生
研究结论
本研究首次揭示了红细胞与表皮系统的整合关系,红细胞外囊泡作为红细胞的代谢产物,可通过血液循环融入皮肤和毛发,既为其提供结构所需的血红蛋白、角蛋白、脂质等关键物质,维持皮肤屏障稳态,又能通过调控Wnt/β-catenin信号通路促进毛发再生。临床研究结果表明自体红细胞外囊泡是治疗雄激素性脱发的有效手段,为毛发再生相关疾病提供了安全、便捷的新治疗策略。
参考文献
Cao Z, Li P, Zhang M, Cai S, Li N, Luo M, Li Y, Wu H, Mao X, Ren R, Xie H, Shi S. Erythrocyte Extracellular Vesicles Amalgamate into the Hair and Skin to Maintain Homeostasis. J Extracell Vesicles. 2025 May;14(5):e70080. doi: 10.1002/jev2.70080. PMID: 40314064; PMCID: PMC12046290.
工程化红细胞来源细胞外囊泡用于Dox与siIDO1递送,提高急性髓系白血病的靶向化学-免疫联合治疗效果
编译者:蔡智 审校者:黄远帅
背景
急性髓系白血病(AML)是一种进展迅速、预后较差的血液肿瘤,传统化疗虽能诱导部分患者缓解,但难以根治,免疫治疗的整体效果也因肿瘤免疫原性低而受到限制。近期研究发现,白血病细胞可通过上调 IDO1,消耗必需氨基酸色氨酸并积累免疫抑制代谢物犬尿氨酸,从而削弱 T 细胞功能、逃避免疫系统。如何既增强白血病细胞的免疫原性,又抑制其免疫逃逸,是提升免疫治疗效果的关键。值得注意的是,阿霉素(Dox)等化疗药物能够诱导免疫原性细胞死亡(ICD),促进抗原呈递与 T 细胞激活;而抑制 IDO1 则可逆转免疫抑制环境。二者若能精准协同,有望实现“化疗+免疫”双重打击。红细胞来源的细胞外囊泡(REVs)具有良好的生物相容性和天然靶向特性,是极具潜力的药物递送工具。基于此,构建了可同时递送 Dox 和 siIDO1 的工程化 REVs(REVs-Dox/siIDO1-P9),能够特异识别并进入白血病细胞,在体内诱导 ICD、抑制 IDO1,协同激活抗白血病免疫反应。在小鼠模型中,这一系统显著促进树突状细胞成熟、增强 T 细胞功能并抑制白血病进展,展示出强大的化疗-免疫级联治疗潜力。
主要结果
1.构建的 REVs-Dox/siIDO1-P9 在经多项表征后显示出良好的理化稳定性。REVs具有留典型胞外囊泡标志蛋白(ALIX、TSG101)、红细胞脂筏膜蛋白(Flotillin-2、STOM)及红细胞特异性蛋白(HBA),同时继续表达红细胞来源 EV 的特征性标志 GPA,而不含内质网及高尔基体相关蛋白(CANX、GM130)。β-actin 几乎不可检测,提示纯化过程有效去除了细胞碎片(图1A)。TEM 与 NTA 显示 REVs 维持杯状囊泡形态,虽在装载 Dox 和 siIDO1 后粒径由约 157 nm 略增至约 171 nm,但整体结构完整、形态一致;Zeta 电位也由 ?9.89 mV 保持在 ?9.69 mV,表明表面电性未发生实质改变(图1B–E)。进一步的血清稳定性实验显示,REVs-Dox/siIDO1-P9 在 PBS 或血清中孵育 7 天后粒径均未发生明显变化(图1F)。因此,最终选用的 REVs-Dox/siIDO1-P9 兼具结构稳定性与良好生理环境耐受性,可满足后续在体药物递送与功能研究的需求。
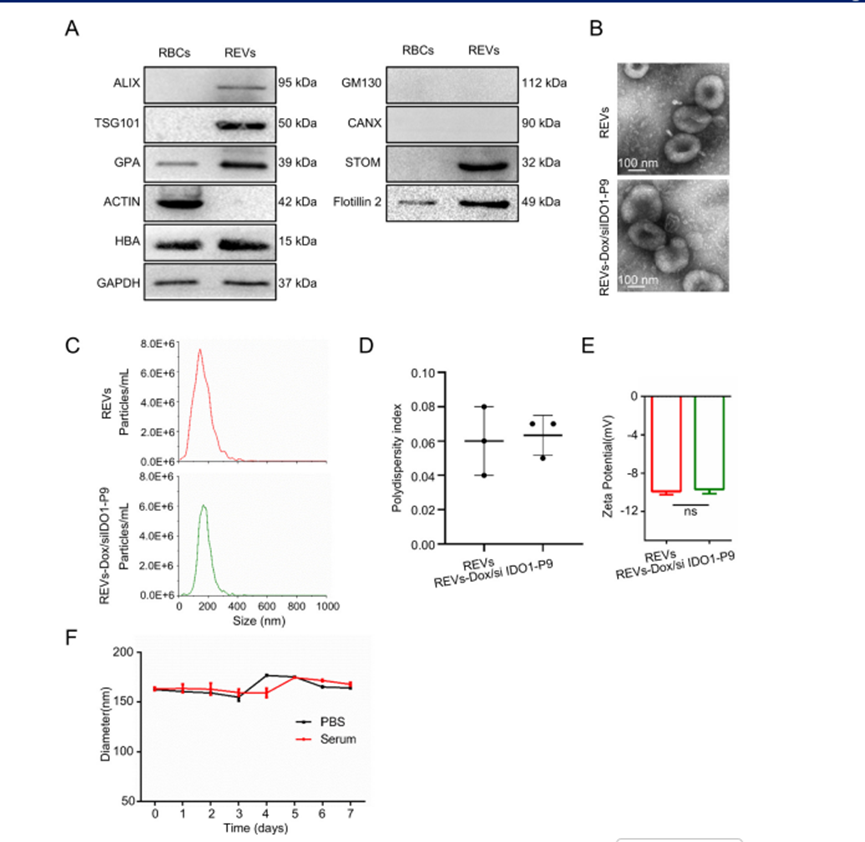
图 1|REVs-Dox/siIDO1-P9 的构建与表征
2.P9 修饰显著(REVs-Dox/siIDO1-P9)提升了REVs在体外对白血病细胞的靶向摄取与治疗效应。结果显示,与乱序肽Pscr修饰的囊泡相比,REVs-Dox/siIDO1-P9在THP-1、C1498细胞及AML原代白血病细胞中均表现出更高的内吞效率(图2A)。进一步的CLSM成像证实,P9可增强DiO标记的REVs在CLL-1阳性AML细胞中的摄取,而对CLL-1阴性的K562细胞无明显作用;游离P9的预处理可削弱该靶向效果,提示摄取依赖P9–CLL-1结合(图2B)。在相同剂量条件下,REVs-Dox/siIDO1-P9对白血病细胞的细胞毒性与游离Dox相当,而REVs-Dox/siIDO1-Pscr的杀伤能力明显较弱,说明靶向性是细胞毒性提升的关键因素(图2C)。同时,REVs-Dox/siIDO1-P9诱导的细胞凋亡率显著高于Pscr对照组(图2D)。两种囊泡均可下调白血病细胞中的IDO1,但P9修饰囊泡的抑制效果更为明显(图2E–G)。因此,P9的表面修饰不仅提高了囊泡的摄取效率,还增强了其促凋亡作用和对 IDO1 的抑制能力,为后续抗白血病治疗奠定了更优的体外效果。
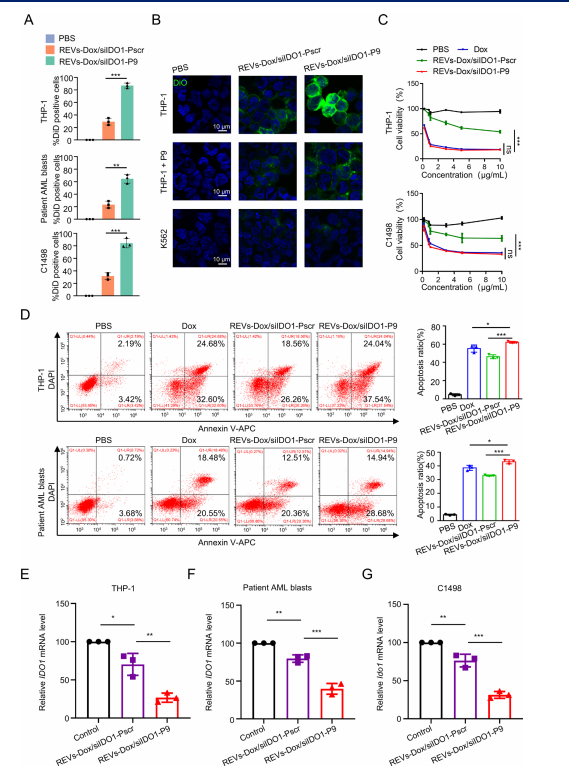
图 2|REVs-Dox/siIDO1-P9 在体外被白血病细胞高效摄取
3.P9修饰显著增强了REVs 在体内对白血病细胞的靶向递送能力,并有效发挥其功能。在骨髓中,P9 的加入使 DiD? THP-1细胞的比例由 29.0% 显著提升至 68.3%;在外周血中,该比例也由29.3%上升至64.2%(图3B)。类似的增强趋势同样出现在脾脏和肝脏,提示 P9 能够促进REVs在多组织白血病病灶中的富集(图3B)。进一步检测发现,在给予治疗24 h后,无论是在AML异种移植模型还是同系移植模型中,来自骨髓、肝脏和脾脏的白血病细胞均呈现IDO1表达水平显著下降(图3C)。因此,最终选用的REVs-Dox/siIDO1-P9不仅能够在体内实现对白血病细胞的高效定向递送,还可在多器官内有效下调IDO1,为发挥体内抗白血病作用提供了关键保证。
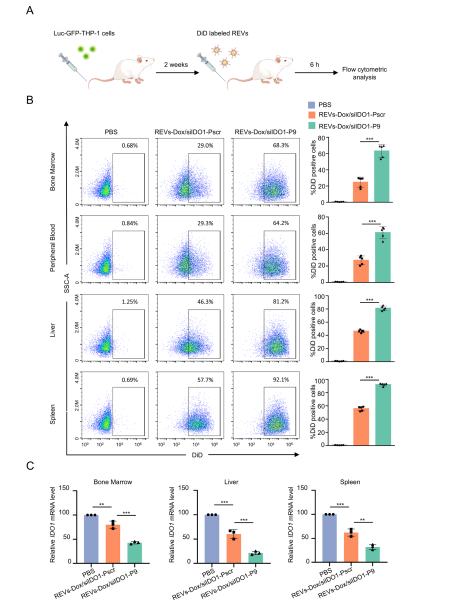
图 3|REVs-Dox/siIDO1-P9 在体内可被有效递送至白血病细胞
4.REVs-Dox/siIDO1-P9 能够有效诱导白血病细胞发生免疫原性细胞死亡(ICD)。在处理THP-1细胞后,可观察到显著增强的细胞表面CRT暴露(图4A),并伴随胞外ATP与HMGB1释放的大幅增加(图4B、C)。与游离Dox相比,REVs-Dox/siIDO1-P9诱导的CRT、ATP和HMGB1 水平均更高,表明其更强的ICD诱导能力可能源于更高的细胞内递药效率。类似结果同样出现在患者来源的AML原代白血病细胞中,其中CRT暴露及 ATP、HMGB1释放均显著升高(图4D、E)。进一步功能验证显示,REVs-Dox/siIDO1-P9处理后的AML原代细胞显著提高了成熟DC的比例(59.2% vs. 50.6%,图4F、G)。因此,REVs-Dox/siIDO1-P9 通过诱导 ICD 不仅增强了白血病细胞的免疫原性,也为后续免疫应答的激活奠定了关键基础。
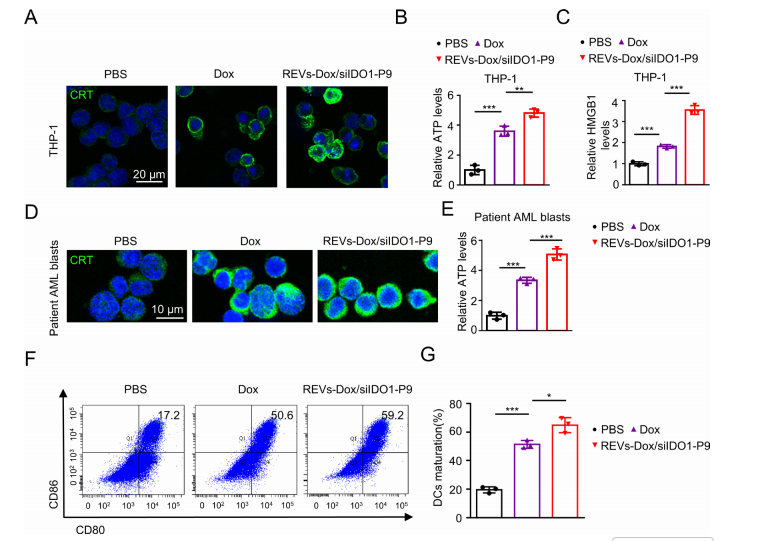
图 4|REVs-Dox/siIDO1-P9 诱导免疫原性细胞死亡(ICD)的作用
5.REVs-Dox/siIDO1-P9 在体内展现出优异的AML抑制效果。在白血病负荷相当的小鼠模型中,PBS组与空载REVs组的生物发光信号广泛分布于骨髓、肝脏及脾脏(图5B)。相比之下,单一递送Dox或siIDO1的REVs-Dox/siNC-P9与REVs-siIDO1-P9均可一定程度降低白血病负荷(图5B)。值得强调的是,REVs-Dox/siIDO1-P9组表现出最为显著的抑制效果,其生物发光信号最低,显示双药联合作用于REVs平台后的明显协同性(图5B)。进一步检测显示,在骨髓、肝脏及脾脏中,该组 GFP? C1498细胞的比例均最低(图5C),与其最强的体内抑瘤能力相一致。组织学分析表明,REVs-Dox/siIDO1-P9可有效防止因白血病浸润导致的脾脏肿大,并明显改善红髓及白髓结构破坏(图5D)。此外,接受该治疗的小鼠体重保持稳定,且生存期显著延长(图5E、F)。因此,REVs-Dox/siIDO1-P9在体内可实现对白血病细胞的高效清除和疾病进程的显著延缓,展现出优越的AML综合抑制效果。
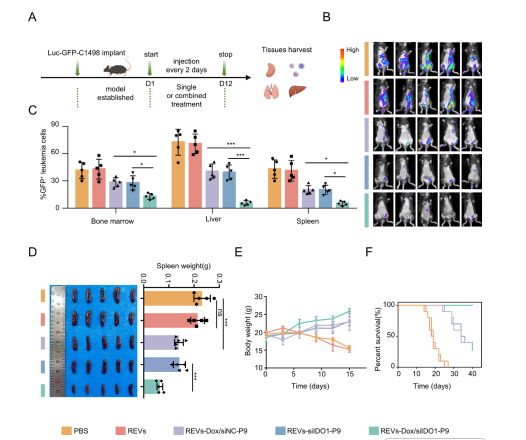
图 5|REVs-Dox/siIDO1-P9 在体内的抗肿瘤疗效
6.REVs-Dox/siIDO1-P9 在体内能够显著激活免疫系统,并增强抗白血病免疫反应。与 PBS 或空载 REVs 组相比,单一载 Dox 的 REVs-Dox/siNC-P9 可将成熟 DC 的比例提升至 20.5%,而 REVs-Dox/siIDO1-P9 则进一步显著提高至约 23.2%,提示双重递送体系可协同促进 DC 成熟(图6A)。相应地,骨髓中 CD8? T 细胞比例在 REVs-Dox/siIDO1-P9 处理后达到最高(15.2%),表明化疗-免疫级联治疗可有效促进效应性 T 细胞向病灶浸润(图6B)。此外,该处理显著增强肿瘤浸润性 CD8? T 细胞的活化与增殖能力(图6C、D)。值得注意的是,载 siIDO1 的 REVs(REVs-siIDO1-P9)能够降低 PD-1? 与 TIM-3? CD8? T 细胞比例,提示 siIDO1 干预可缓解 T 细胞耗竭(图6E、F)。因此,REVs-Dox/siIDO1-P9 不仅实现了对白血病细胞的直接杀伤,还通过免疫激活和逆转 T 细胞耗竭,增强了体内抗白血病免疫效应,为化疗-免疫联合治疗提供了可靠策略。
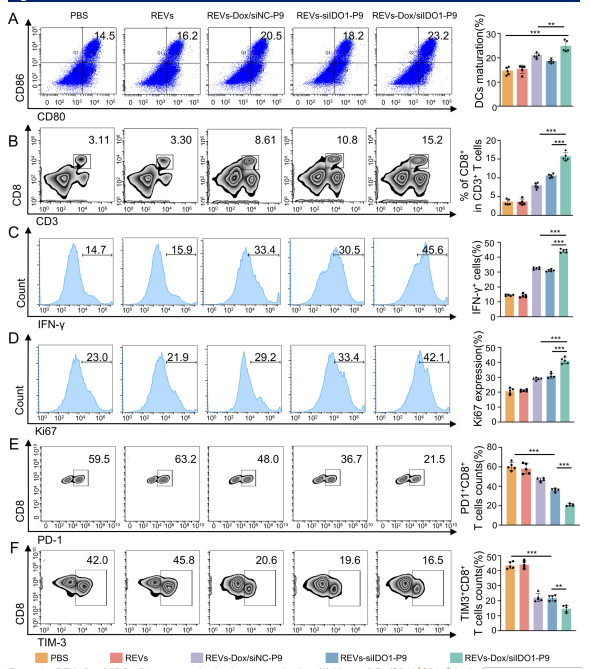
图 6|REVs-Dox/siIDO1-P9 促进体内免疫激活
7. REVs-Dox/siIDO1-P9 在 AML 治疗中表现出良好的生物安全性。对主要脏器(脾脏、肝脏、心脏、肺和肾脏)进行 H&E 染色显示,各处理组均未观察到明显的炎症反应或组织损伤(图7A)。同时,血液学及血液生化指标均保持在正常范围内,未出现明显异常(图7B、C)。这些结果表明,REVs-Dox/siIDO1-P9 不仅具有优异的抗白血病疗效,还具备良好的体内安全性,为其在 AML 治疗中的潜在应用提供了坚实依据。
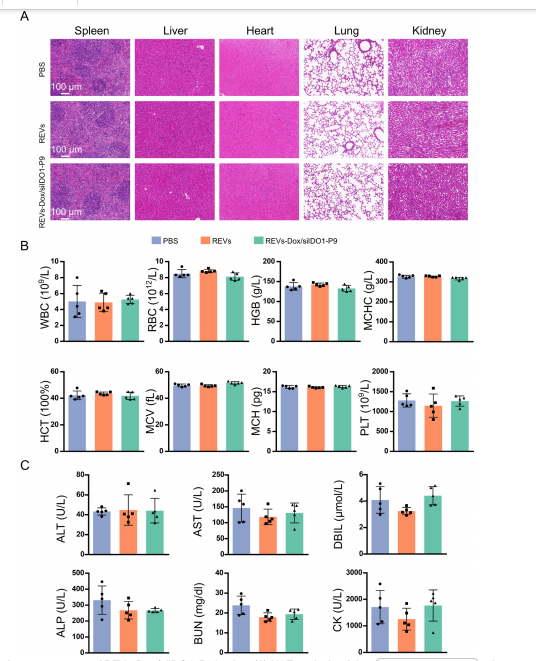
图 7|REVs-Dox/siIDO1-P9 的体内生物安全性评估
结论
本研究开发了一种基于红细胞来源囊泡(REVs)的双重递送系统(REVs-Dox/siIDO1-P9),能同时将化疗药物 Dox 和免疫调控分子 siIDO1 精准送入白血病细胞。该系统通过增强肿瘤细胞免疫原性、促进树突状细胞成熟并增加 CD8? T 细胞浸润,实现强效抗白血病免疫反应。实验显示,在 AML 小鼠模型中,它不仅显著抑制白血病进展,还降低了非靶组织毒副作用。未来,这一策略有望拓展应用于其他肿瘤的化疗-免疫联合治疗。
参考文献:
Liu Y, Hu J, Shu Y, Li G, Jin F, Ren J, et al. Engineered red blood cell extracellular vesicles for delivery of Dox and siIDO1 enhance targeted chemo-immunotherapy of acute myeloid leukemia. J Immunother Cancer. 2025 Jul 15;13(7):e011148. doi: 10.1136/jitc-2024-011148. PMID: 40664450; PMCID: PMC12265820.
红细胞外囊泡递送治疗性 siRNA 靶向骨骼肌,为癌症恶病质治疗提供新策略
编译者:王育 审校者:黄远帅
一、背景
癌症恶病质是一种以骨骼肌进行性丢失为核心特征的多因素综合征,影响 80% 的晚期癌症患者,导致患者体质虚弱、生活质量下降,更是 20%-30% 癌症患者的主要死亡原因。目前尚无标准治疗方案,传统营养支持、促食欲药物等效果有限,新型治疗药物因递送系统效率低、毒性大或靶向性不足,相关临床试验多以失败告终。肌抑素(Mstn)是骨骼肌生长分化的负调控因子,抑制其表达可改善肌肉萎缩,但现有 Mstn 抑制剂存在脱靶效应和非肌肉相关不良反应;丙二酰辅酶 A 脱羧酶(Mlycd)驱动癌症恶病质状态下骨骼肌脂肪酸代谢紊乱,加剧肌肉消耗,二者均为潜在治疗靶点。小干扰 RNA(siRNA)可序列特异性沉默靶基因,但其稳定性差、递送困难,现有脂质体、阳离子聚合物等递送系统存在安全性隐患。红细胞来源外囊泡(RBCEVs)具有生物安全性高、生物相容性好、易获取、可规模化制备等优势,为 siRNA 靶向递送提供了理想载体。
二、主要结果
1. RBCEVs 的靶向递送特性
肌内注射后,RBCEVs 可通过内吞作用被肌纤维高效摄取,且极少渗漏至血液循环及其他器官,实现肌肉特异性递送;RBCEVs 能有效装载 Mstn siRNA 和 Mlycd siRNA(装载效率分别达 80.8% 和 81.7%),并保护 siRNA 免受核酸酶降解。体外及裸鼠体内实验证实 RBCEVs 通过内吞作用被肌细胞摄取,且荧光信号仅局限于注射部位肌肉(图1A-C);C57BL/6 小鼠肌内注射后,CFSE 标记的 RBCEVs 被多个肌纤维内化,siMstn-4-RBCEVs 可显著抑制 Mstn 表达(图1D-E)。
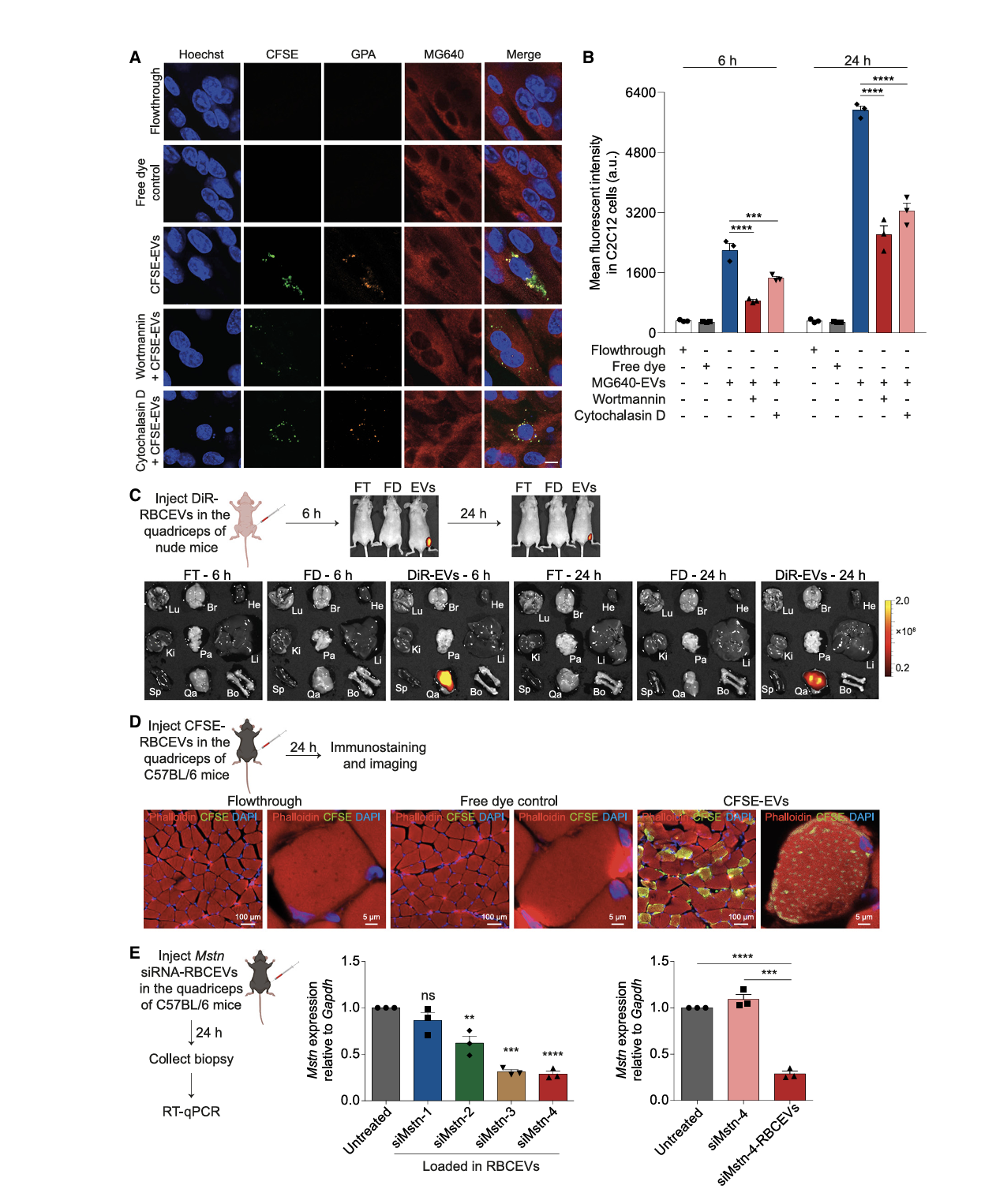
图 1 RBCEVs 携带 siRNA 经肌内注射被肌纤维内化
2. 单一靶点 siRNA 的治疗效果
Mstn siRNA的治疗作用:装载 Mstn siRNA 的 RBCEVs 肌内注射可显著抑制小鼠骨骼肌 Mstn 表达,促进肌肉生长,使肌肉重量增加 24.2%(图2B-D);通过 qPCR 和 Western blot 证实 Mstn mRNA 及蛋白表达被有效抑制(图2G-H)。在肺癌恶病质小鼠模型中(图3A),siMstn-EVs 可维持前肢、后肢肌肉大小(图3B-C);研究证实肌肉质量、肌纤维横截面积增加,且显著延长小鼠生存期(图3D-G)。
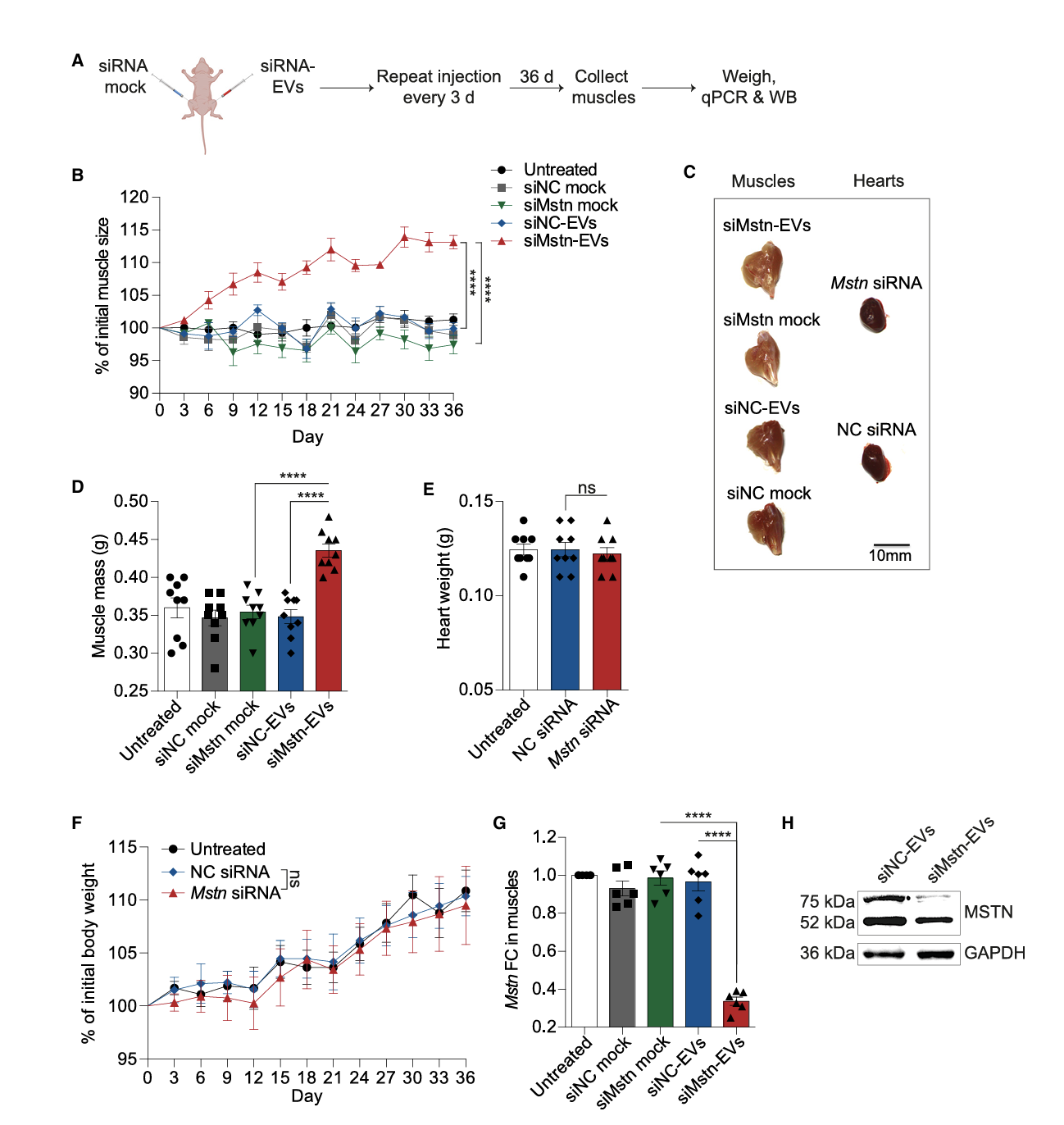
图 2 RBCEV 介导的 Mstn siRNA 递送促进肌肉生长
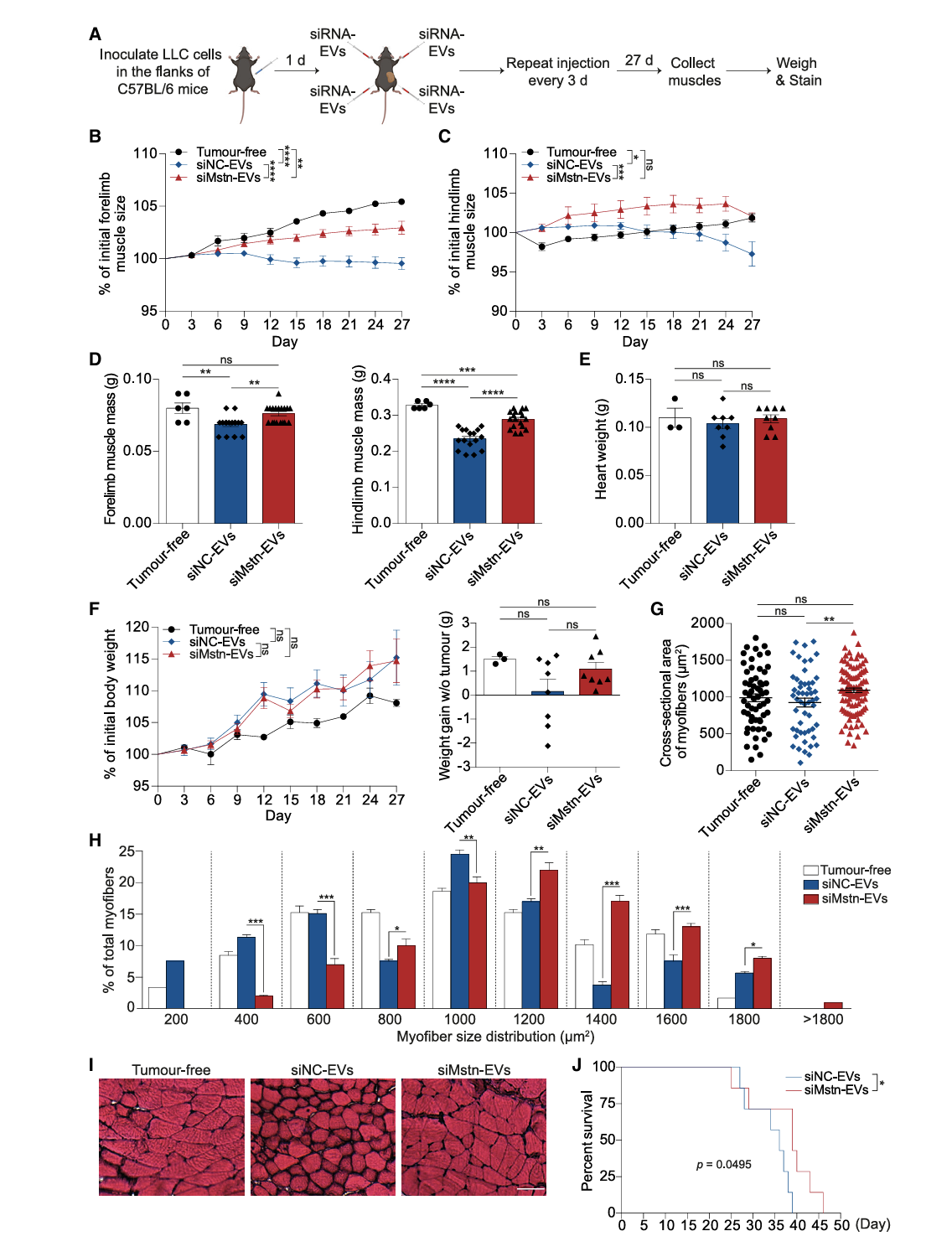
图 3 RBCEV 介导的 Mstn siRNA 改善肺癌恶病质小鼠肌肉萎缩
Mlycd siRNA 的治疗作用:装载 Mlycd siRNA 的 RBCEVs 同样能促进肌肉生长,改善恶病质小鼠的肌肉消耗,增加去瘤后的体成分重量。研究筛选出抑制效果最佳的 siMlycd-1(图4A);图4B为实验设计;研究证实 Mlycd 蛋白表达被抑制,肌肉重量、大小显著增加(图4C-E);实验显示肌纤维横截面积显著扩大,且大尺寸肌纤维(2400-3800μm2)的比例明显升高(图 4H-J)。图5A为治疗方案;研究显示 siMlycd-EVs 可维持恶病质小鼠前肢、后肢肌肉量(图5B-D);证实体成分重量增加,且无明显心脏毒性(图5E-F)。
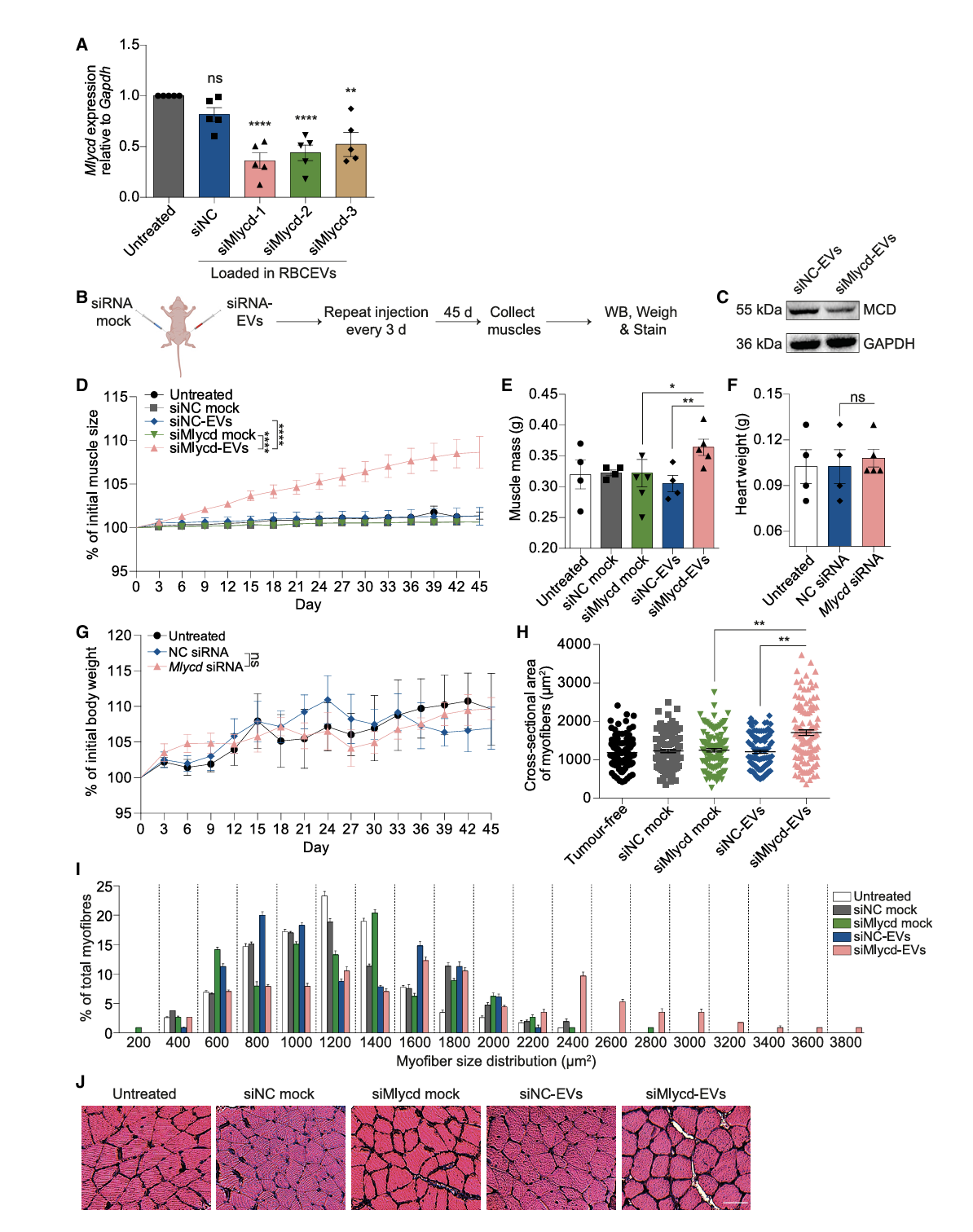
图 4 RBCEV 介导的 Mlycd siRNA促进肌肉生长 注:
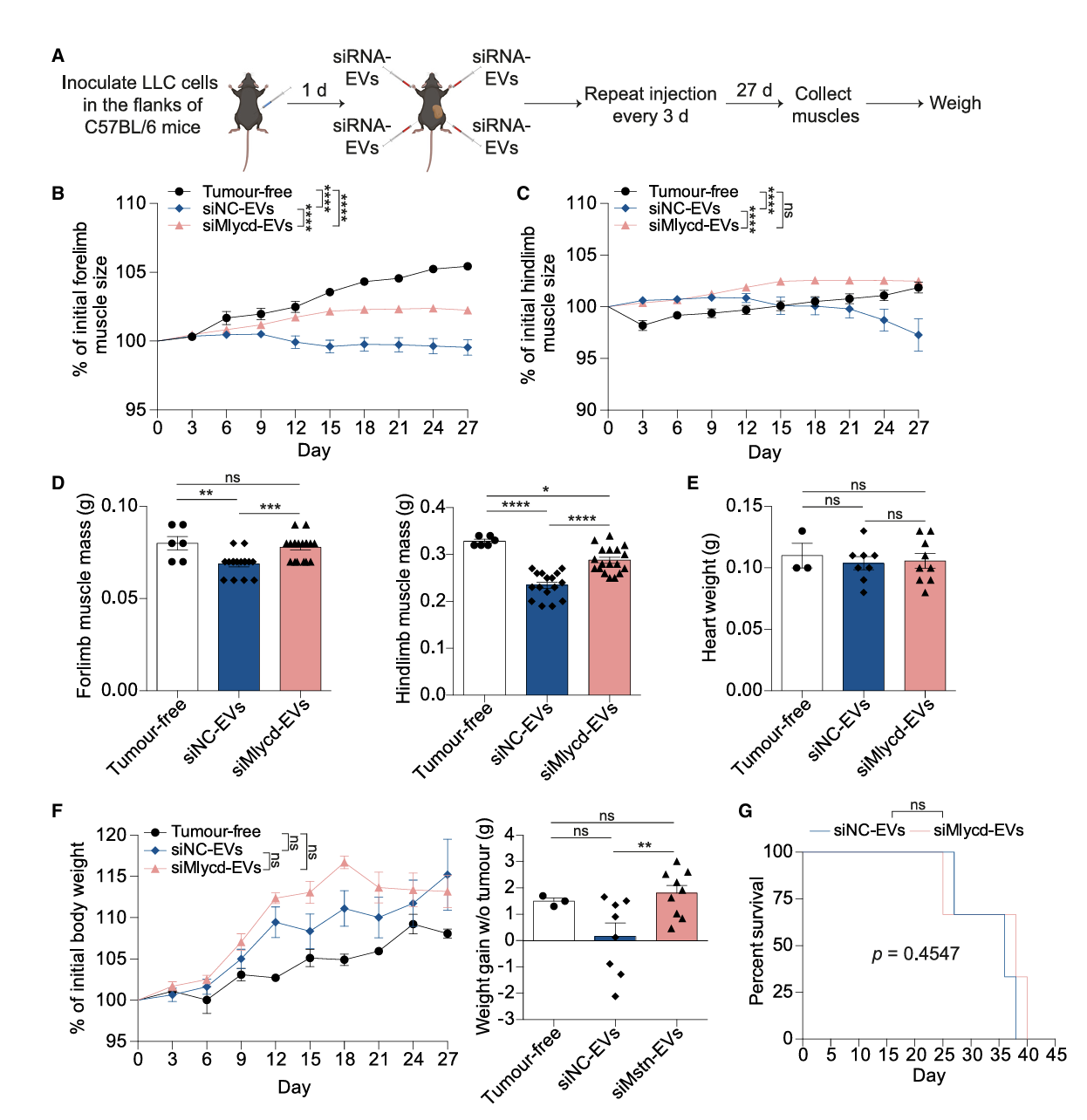
图 5 RBCEV 介导的 Mlycd siRNA 抑制癌症恶病质相关肌肉丢失
3. 联合靶向治疗的协同效应
同时装载 Mstn siRNA 和 Mlycd siRNA 的 RBCEVs,治疗效果优于单一靶点治疗,研究显示,联合治疗组的肌肉大小增加更显著,肌肉质量和肌纤维横截面积均优于单一靶点治疗(图6B-G);同时可显著延长恶病质小鼠生存期,并有效改善前肢握力(图6J-K)。
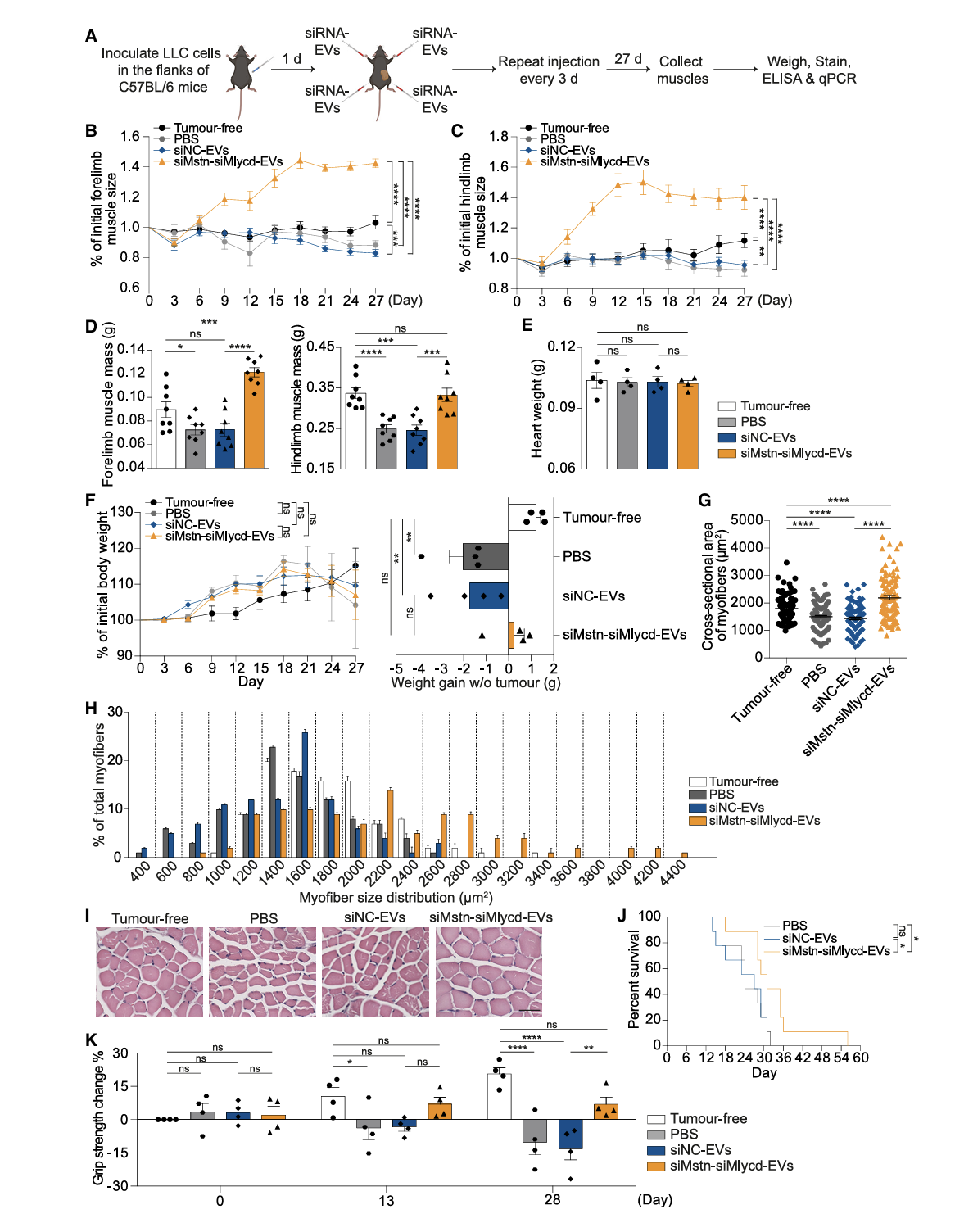
图 6 Mstn siRNA 与 Mlycd siRNA 联合治疗增强恶病质改善效果
4. 安全性优势
治疗剂量下,RBCEVs 递送系统未引起肝肾功能损伤,血清肝肾功能相关指标(ALT、AST、肌酐等)均无异常(图 7A-B、7D-E);也未引发全身炎症反应(图 7G),且血清促卵泡激素(FSH)水平与对照组无差异,避免了传统 Mstn 抑制剂的脱靶效应(图 7C、F)。
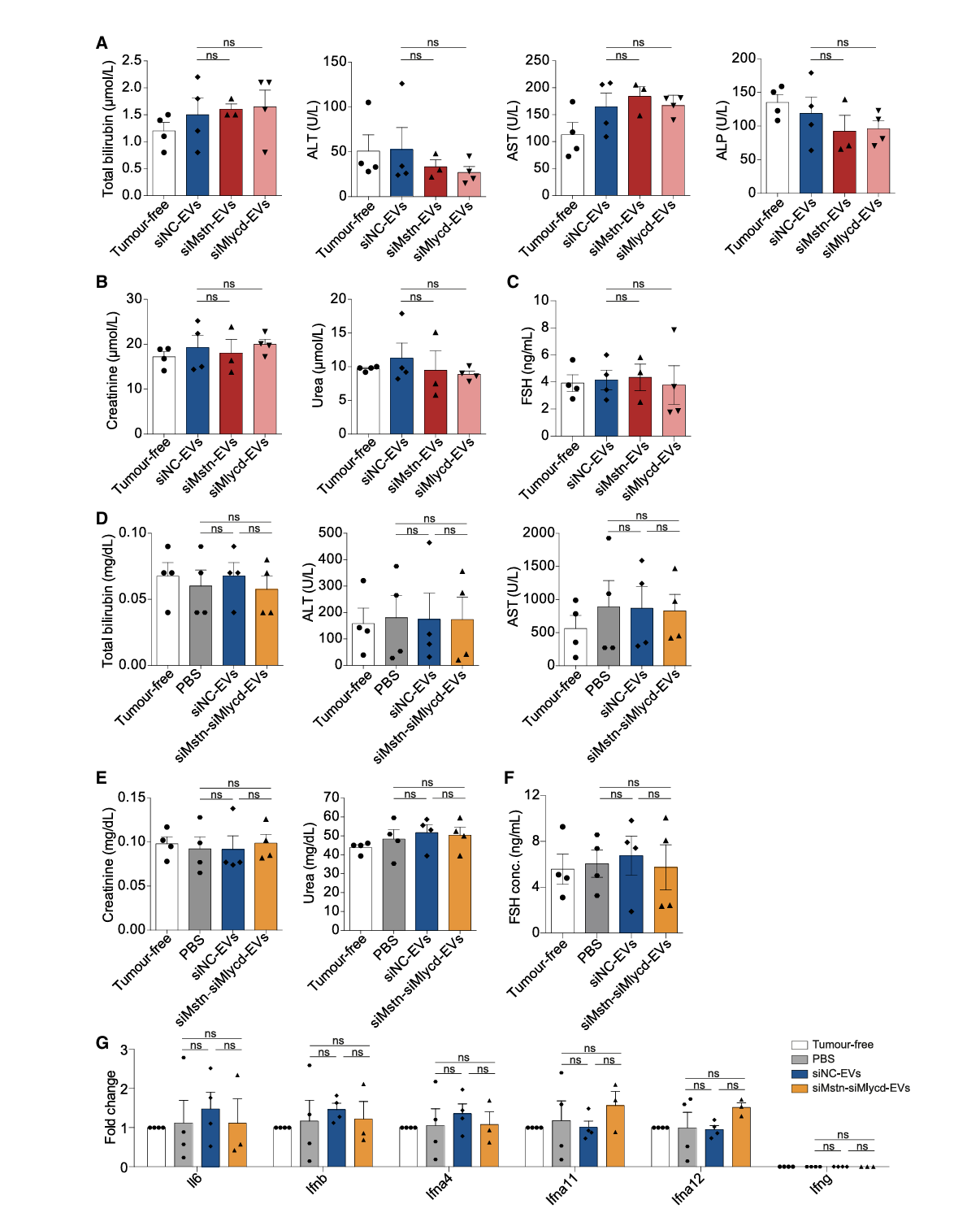
图 7 RBCEV 递送 siRNA 的安全性验证
三、结论
本研究证实,红细胞来源外囊泡(RBCEVs)是一种安全高效的 siRNA 递送载体,通过肌内注射可实现治疗性 siRNA 向骨骼肌的特异性递送。靶向 Mstn 或 Mlycd 的 siRNA-RBCEVs 复合物能有效改善癌症恶病质相关肌肉萎缩,二者联合使用效果更优。该策略不仅解决了 siRNA 递送的稳定性和靶向性难题,还通过肌肉特异性递送降低了治疗剂量与毒性风险,为癌症恶病质及其他肌肉退行性疾病提供了安全有效的新治疗方向。
四、文献来源
Boya Peng, Yuqi Yang, Zhiyuan Wu, et al. Red blood cell extracellular vesicles deliver therapeutic siRNAs to skeletal muscles for treatment of cancer cachexia[J]. Molecular Therapy, 2023, 31(5): 1418-1436. https://doi.org/10.1016/j.ymthe.2023.03.036